超高效液相色谱-串联质谱法测定动物源基质中地塞米松的残留量
2021-12-24 17:03:40 来源: 食品安全导刊
杨毅青,王莉佳,马增辉,王 祺
(山西省食品药品检验所,山西太原 030001)
摘 要:目的:建立超高效液相色谱-串联质谱法测定牛奶和鸡蛋不同基质中地塞米松残留量的分析方法。方法:样品经乙酸-乙酸钠和甲醇溶液提取,固相萃取柱净化后,以甲醇-0.1%甲酸溶液为流动相进行梯度洗脱,采用电喷雾负离子模式电离,多反应监测(MRM)模式进行采集,内标法定量。结果:地塞米松在0~44.191 4 ng/mL范围内线性关系良好,相关系数为0.999 9,平均回收率为70.53%~118.25%,为3.5%~7.0%。结论:该方法快捷、简便、回收率高,重现性好,可用于不同动物源基质中地塞米松的残留量分析。
关键词:地塞米松;超高效液相色谱-串联质谱法;动物源性食品
Determination of Dexamethasone Residues in Animal Matrix by High-Performance Liquid Chromatography-Tandem Mass Spectrometry
YANG Yiqing, WANG Lijia, MA Zenghui, WANG Qi
(Shanxi Institute for Food and Drug Control, Taiyuan 030001, China)
Abstract: Objective: To establish a method for the determination of dexamethasone residues in milk and eggs by ultra performance liquid chromatography-tandem mass spectrometry (UPLC-MS/MS). Methods: The samples were extracted by acetic acid-sodium acetate and methanol solution, purified by spe column, and eluted by gradient elution with methanol-0.1% formic acid solution as mobile phase. The samples were ionized by electrospray ionization in negative ion mode, and collected by multiple reaction monitoring (MRM) mode, and quantified by internal standard method. Results: Dexamethasone had a good linear relationship in the range 0~44.191 4 ng/mL , the correlation coefficient () was 0.999 9. The recoveries were 70.53%~118.25%, and with the relative standard deviations () of 3.5%~7.0%. Conclusion: This method is rapid, simple, good recovery and good reproducibility, which is suitable for rapid determination of dexamethasone residues in different substrates of animal origin.
Keywords: dexamethasone; ultra-performance liquid chromatography-tandem mass spectrometry; animal derived food
地塞米松又名氟美松、氟甲强地松龙、德沙美松,是糖皮质类激素。其衍生物有氢化可的松、泼尼松等,其药理作用主要是抗炎、抗毒、抗过敏、抗风湿,临床使用较广泛[1-2]。而在兽医治疗中被广泛应用于治疗母畜代谢病,是畜禽饲养中普遍的药物之一[3]。激素的频繁使用会在畜禽体内残留,不仅给动物源食品安全带来隐患,而且对人们的健康及环境危害严重[4]。因此,世界各国严格禁止地塞米松作为生长激素使用,且限制该药物用于动物源性食品中,并提出了严格的限量要求[5]。
目前,国内外有关地塞米松残留的检测方法较多,主要采用酶联免疫法、液相色谱法、液相色谱-串联质谱法、超液相色谱-串联质谱法、气质联用法等。本研究参照国家标准GB/T 21981—2008[6],建立了一种快捷、简便、回收率好的超高效液相色谱-串联质谱法快速检测不同动物源基质中地塞米松残留量的方法,为快速高效检测动物源性食品中地塞米松的残留提供参考。
1 材料与方法
1.1 材料、试剂及仪器
1.1.1 试验样品
新鲜牛奶、鸡蛋,均购置于某超市。
1.1.2 主要试剂
地塞米松标准品(中国食品药品检定研究院,含量99.8%);氢化可的松-d3(阿尔塔科技有限公司,含量98.0%);甲醇、二氯甲烷、甲酸(美国Fisher公司,色谱纯);乙酸、乙酸钠(NaAC·4H2O)(国药集团,分析纯);β-葡萄糖醛酸酶4.5 U/mL(德国默克公司);实验室一级超纯水。ENVI-Carb固相萃取柱(500 mg/6 mL)和氨基固相萃取柱(500 mg/6 mL)(艾杰尔科技公司)。
1.1.3 仪器与设备
LCMS-8050液质联用仪(日本岛津公司);UB-7pH计(丹佛仪器);V2S025涡旋混合器(德国ZKA);HC-3018离心机(安徽中科中佳科学仪器);氮吹浓缩仪(天津安特塞恩斯)。
1.2 试验方法
1.2.1 液相条件
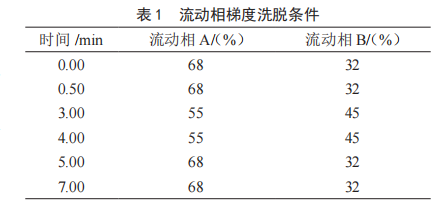
色谱柱:YMC C18(100 mm×2.1 mm,3 µm);流动相:0.1%甲酸水溶液+甲醇溶液,梯度洗脱,见表1;流速:0.2 mL/min;柱温:40 ℃;进样量:10 µL。
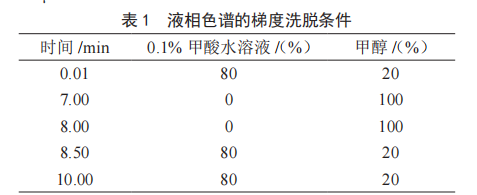
1.2.2 质谱条件
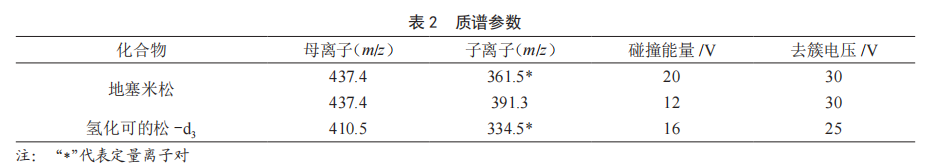
离子化模式:ESI-;质谱扫描模式:多反应检测(MRM);电喷雾电压:-3 000 V;离子源温度:300 ℃;加热气流量:10 L/min;干燥气流量:10 L/min;辅助气压力:60 psi;其他质谱参数见表2。
1.2.3 提取与净化
称取均质试样5 g,置于50 mL离心管中,准确加入内标工作液100 µL和10 mL乙酸-乙酸钠缓冲溶液,涡旋混匀,再加入β-葡萄糖醛酸酶100 µL,于(37±1)℃振荡酶解12 h。取出冷却至室温,加入25 mL甲醇超声提取30 min,0~4 ℃下,10 000 r/min离心10 min。将上清液转入洁净烧杯,加水100 mL,混匀后待净化。依次用6 mL二氯甲烷-甲醇溶液,6 mL甲醇,6 mL水活化ENVI-Carb固相萃取柱。提取液以2~3 mL/min的速度上样于活化过的ENVI-Carb固相萃取柱。将小柱减压抽干。用6 mL二氯甲烷-甲醇溶液活化氨基固相萃取住。将活化好的氨基柱串联在ENVI-Carb固相萃取柱下方。用6 mL二氯甲烷-甲醇溶液洗脱并收集洗脱液,取下ENVI-Carb柱,再用2 mL二氯甲烷-甲醇溶液洗氨基柱,洗脱液在微弱的氮气流下吹干,用1 mL甲醇-水溶液溶解残渣,供仪器测定。用空白样品,不加入内标,按上述步骤制备空白样品提取液。
1.2.4 标准溶液配制
(1)标准储备溶液。地塞米松标准品称量前于105 ℃干燥箱干燥至恒重,经折算相当于11.0479 mg地塞米松的标准品,用甲醇溶解并定容至100 mL棕色容量瓶中,得浓度为110.479 0 µg/mL的标准储备液。此储备液可在-18 ℃以下避光存放12个月。
(2)内标工作液。取适量氢化可的松-d3内标溶液,配制出浓度为100 ng/mL的内标工作液。
(3)标准工作中间液。取适量地塞米松标准储备溶液配制成浓度为1.1047 9 μg/mL的标准工作中间液。
(4)标准工作液。取适量标准储备溶液配制得浓度为110.479 0 ng/mL的标准工作液。
1.2.5 系列标准工作溶液配制
分别取标准工作中间液0 mL、0.015 mL、0.020 mL、0.050 mL、0.100 mL、0.200 mL和0.400 mL,用甲醇定容至10 mL,配制成系列标准工作溶液。标准工作液中含内标浓度为10 ng/mL。
2 结果与分析
2.1 线性关系及定量限
以地塞米松的定量离子峰面积与内标峰面积的比值为纵坐标(y),相应的质量浓度为横坐标(x),绘制标准曲线,得出该样品在0~44.191 4 ng/mL浓度范围内的线性方程为=0.204 1-0.027 6,相关系数=0.999 9,线性良好。取空白样品按照方法定量限(浓度为0.4 µg/kg)水平进行加标试验,制备好的试样溶液上机测定,信噪比大于10,满足检测要求。
2.2 回收率和重复性
取空白样品,添加不同浓度的地塞米松标准溶液进行加标回收试验,其余操作同上述供试品溶液制备,每个浓度平行测定6次,计算加标回收率和重复性,结果见表3。(牛奶和鸡蛋的方法定量限为0.4 µg/kg;最高残留限量分别为0.3 µg/kg和不得检出)。
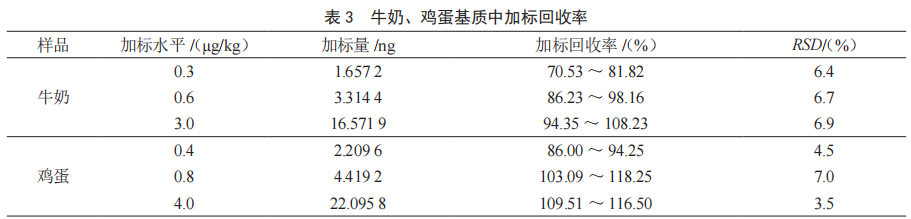
3 结论
本研究通过对不同基质中地塞米松残留量进行质谱分析,建立了超高效液相色谱-质谱联用检测方法,能同时快速检测出牛奶和鸡蛋不同基质中添加的地塞米松残留量,并从线性关系、重复性、回收率、精密度等方面对方法进行了考察,结果表明,该方法测定动物源食品中的地塞米松残留量,方法稳定,数据可靠,为研究动物源食品地塞米松残留量的检测提供了一定的参考依据。
参考文献
[1]郑宇潇.地塞米松在临床肿瘤治疗中的应用进展[J].医学综述,2019,25(17):3491-3496.
[2]GUILLAUME B,KARINE B,VIRGINIE M,et al.Preparation and physicochemical stability of liquid oral dosage forms free of potentially harmful excipient designed for pediatric patients[J].Pharmaceutics,2019,11(4):190.
[3]王永娟,朱善元,刘博,等.地塞米松促进猪繁殖与呼吸综合征病毒致病性[J].江苏农业科学,2016,44(7):293-295.
[4]周军,李红斌,李睿鸿.滥用抗生素对养猪业的危害及应对措施[J].当代畜禽养殖业,2011(6):44-47.
[5]林维宣.各国食品中农药兽药残留限量规定[M].大连:大连海事大学出版社,2003.
[6]中华人民共和国国家质量监督检验检疫总局,国家质量监督检验检疫总局.动物源食品中激素多残留检测方法 液相色谱-质谱/质谱法:GB/T 21981—2008[S].北京:中国标准出版社,2008.
热点推荐
-

使用梅特勒-托利多X光机的五大理由
-

小个头 大营养 禾泱泱有机稻鸭原生小泱胚芽米 金秋喜迎初丰收
-

全球食品创新平台第五期已启动,携手共创安全、健康、绿色的未来
-
特医食品不是药,却是临床治疗的关键支撑
-

“喂饱”体内的益生菌,肠道更健康
-

超高效液相色谱-串联质谱法测定动物源基质中地塞米松的残留量
-
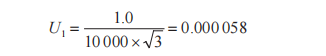
LC-MS/MS法测定蒸馏酒中环己基氨基磺酸钠的不确定度评定
-
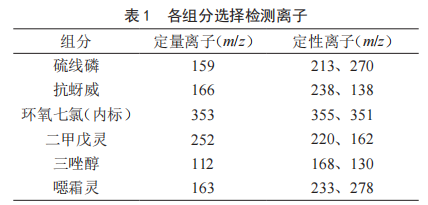
QuEChERS-气相色谱串联质谱法测定蔬菜中5种农药残留
-
高效液相色谱法测定粮油食品中黄曲霉毒素含量
-
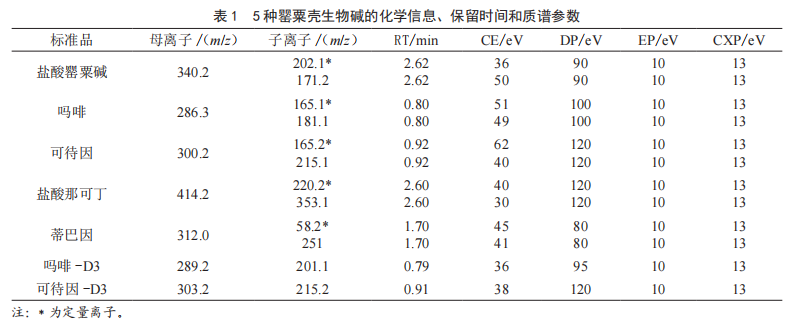
SPE-UPLC-MS/MS法测定方便面及其料包中5种罂粟壳生物碱
-
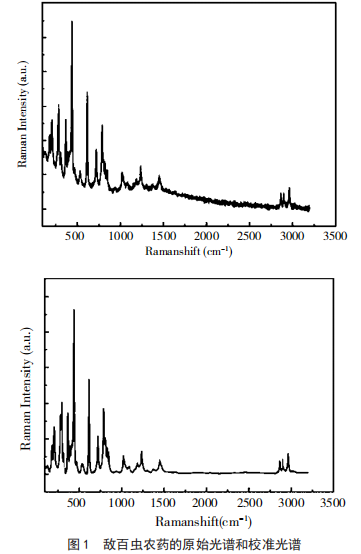
基于拉曼光谱技术的水果残留农药检测方法探讨
-
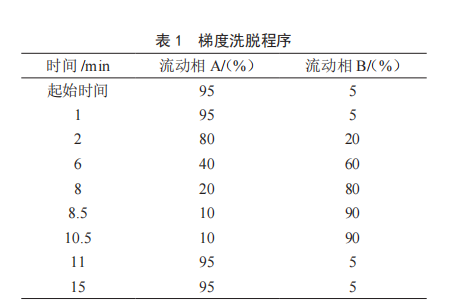
超高效液相色谱-串联质谱法测定β-受体激动剂残留量的研究
-

铜绿假单胞菌快速检测方法的优化研究
-

霉菌酵母快速检测测试片的优化
-

食品检测实验室的内部质量控制方式分析
-
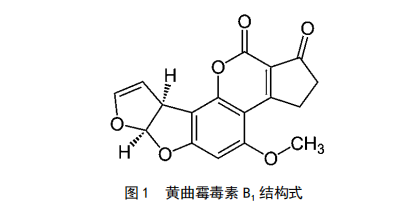
食品中黄曲霉毒素B1检测方法研究
-

多重PCR法检测5种动物源性成分的适用性验证
-
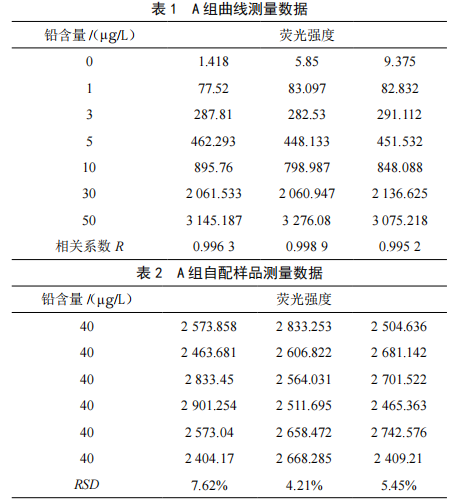
还原剂浓度对氢化物原子荧光法测量饮用水中铅的影响
-
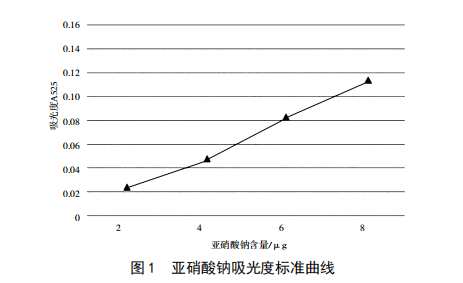
酱菜腌渍类食品亚硝酸盐含量的检测
-
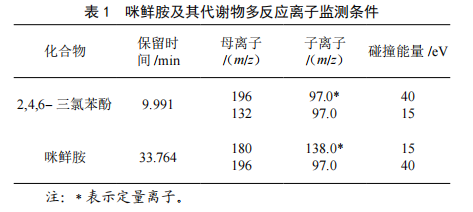
气相色谱-三重四极杆质谱法测定辣椒中咪鲜胺及其代谢物残留量
-
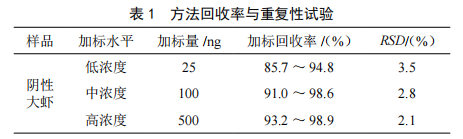
液相色谱-原子荧光法测定水产食品中的甲基汞
-

利用HPLC内标法测定益生菌类保健食品中低聚木糖的含量
-
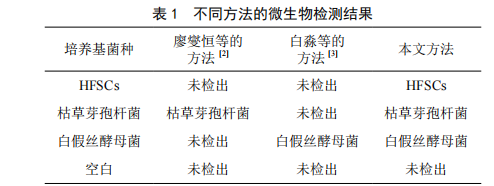
ATP生物荧光增幅法在食品微生物污染检测中的应用
-

高效液相色谱仪、酶标仪和快检仪检测小麦中呕吐毒素的对比分析
-
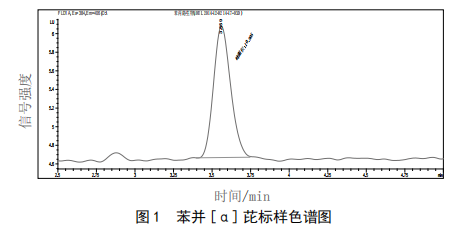
高效液相色谱法测定烤鱼中的苯并[α]芘
-
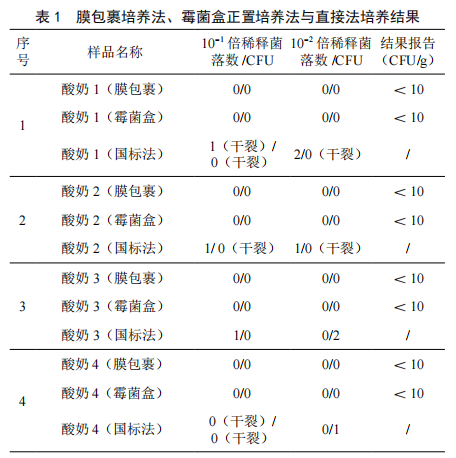
食品中霉菌检测方法的改进研究
-
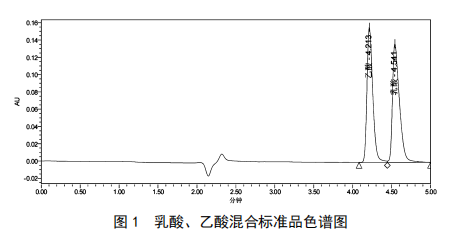
超高效液相色谱法测定不同香型白酒中乳酸和乙酸的含量
-
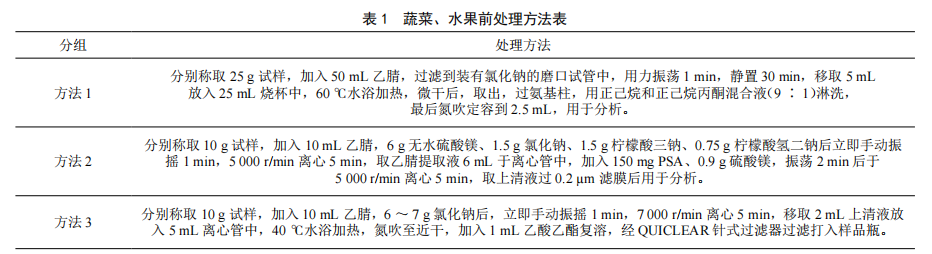
不同前处理方法对蔬菜、水果农药残留GC-MS/MS检测结果的影响分析
-
气相色谱-质谱联用法测定白花蛇舌草中10种有机磷农药残留量
-
基于GC和GC-MS技术检测山茶油掺伪





