食品中大肠菌群检测结果与分析
2021-08-05 16:15:32 来源: 食品安全导刊
董慧明
(辽宁省检验检测认证中心,辽宁沈阳 110036)
摘 要:为了提高微生物实验室大肠菌群的检测能力,辽宁省检验检测认证中心于2019年参加了乳粉中大肠菌群的计数(定量)检测能力验证,依据《食品安全国家标准 食品微生物学检验 大肠菌群计数》(GB 4789.3—2016)进行检验,同时应用3M Petrifilm CC测试片作为对照手段。结果表明,样品CODE TF02240028结果报告为3 100 CFU/g、CODE TF02240028结果报告为4 200 CFU/g,反馈结果满意,值均<2。
关键词:大肠菌群;能力验证;平板计数;3M测试片
大肠菌群是一群能发酵乳糖、产酸产气、无芽孢需氧及兼性厌氧的革兰氏阴性杆菌。大肠菌群与大肠杆菌相似,可以其检出情况来判断食品是否受到了人及温血动物粪便的污染,作为食品、饮用水等卫生指标菌[1]。大肠菌群定量检测为食品微生物实验室常规检测项目,其检测结果的准确性能判定实验室基本能力水平是否达到要求。食品中大肠菌群的检测有着重要意义,可以掌握食品的卫生状况,有利于控制肠道病的爆发传播,及时做出有效的预防措施[2]。
能力验证活动是利用实验室间的比对,按照预先制定的准则评价参加者的能力[3]。为提高实验室食品微生物检测能力,确保出具的检验报告的准确性和科学性,同时完成实验室质量控制和完善实验室管理制度,本实验室报名参加了中国食品药品检定研究院乳粉中大肠菌群的计数(定量)能力验证。本实验依据国家标准《食品安全国家标准 食品微生物学检验 大肠菌群计数》(GB 4789.3—2016)[4]的要求进行实验,同时应用3M Petrifilm CC测试片作为对照手段。
1 材料与方法
1.1 样品
本实验室收到2件待测样品,每件样品由1个菌球及相应奶粉组成,编码分别为CODE TF02240028、CODE TF02240125。检测时每个相同编码的大肠菌群样品和奶粉基质作为1件样品进行检测。以无菌操作打开样品的西林瓶,将西林瓶内小球加入到225 mL 0.85%生理盐水中,充分溶解;然后再将与西林瓶相同编码的奶粉样品加入到上述生理盐水中,充分均质混匀。依此方法,分别对2件样品进行处理,制成1∶10的样品匀液。
1.2 仪器与试剂
电热恒温培养箱(德国Binder公司);A2型生物安全柜(美国NUAIRE公司);生物显微镜(日本Olympus公司);电子天平(瑞士梅特勒-托利多公司);高压灭菌锅(日本Tomy公司);均质器(法国梅里埃公司)。
煌绿乳糖胆盐(brilliant green lactose bile,BGLB)肉汤、结晶紫中性红胆盐琼脂(Violet Red Agar,VRBA)、0.85%无菌生理盐水,均购自北京陆桥技术有限公司;Petrifilm CC大肠菌群测试纸片(美国3M公司)。
1.3 实验方法
依据国家标准《食品安全国家标准 食品微生物学检验 大肠菌群计数》(GB 4789.3—2016)[4]的要求进行实验。同时,用3M大肠菌群测试纸片法作为对照手段进行实验, 每个稀释度做两平行,每片接种量为1 mL,36 ℃培养24 h。
2 结果与分析
2.1 培养计数
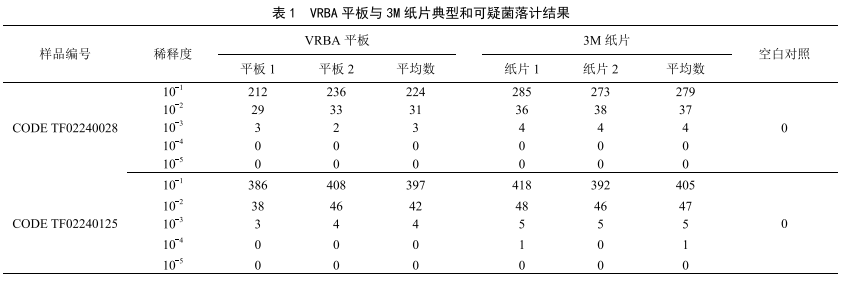
在VRBA平板上选取菌落在15~150 CFU的平板,分别计数平板上出现的典型和可疑菌落,典型菌落为紫红色,菌落周围有红色的胆盐沉淀环,菌落直径为0.5 mm,或更大[4]。大肠菌群菌落在3M大肠菌群测试片上生长产酸使培养基颜色变红变深,目标菌落为红色菌落并且周围有气泡产生,计数结果见表1。
2.2 确证实验
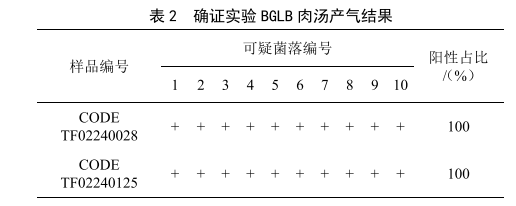
从10-2稀释度的VRBA平板上挑取10个典型和可疑菌落(不同类型),用无菌接种针取挑取菌落的菌体分别接种于BGLB肉汤管中,36 ℃培养24~48 h,观察产气情况,凡BGLB肉汤管产气,即可报告为大肠菌群阳性(+)[4],需要注意的是如果接种前BGLB导管内有气泡,应该先排除以免影响结果。两个样品选取的所有典型和可疑菌落均为大肠菌群,见表2。
2.3 大肠菌群平板计数的报告
经最后证实为大肠菌群阳性的试管比例乘以相应稀释度VRBA平板计数菌落数,再乘以稀释倍数,即为样品中大肠菌群结果报告数,单位为CFU/g。样品编号CODE TF02240028结果报告为3 100 CFU/g,样品编号CODE TF02240028结果报告为4 200 CFU/g。
2.4 实验结果反馈
经能力验证组织机构反馈,本实验室CODE TF02240028大肠菌群的检测结果为3.491,指定值为3.732,值为1.16;CODE TF02240125大肠菌群的检测结果为3.623,指定值为3.732,值为0.52;值均<2,两个样品的结果评价为满意。
3 结论与讨论
本次大肠菌群能力验证结果报告与指定值相比数值偏低,分析原因可能是:①人员操作时间过长,样品处理后应立即进行检验,操作时间过长会导致菌体死亡,造成实验结果偏低;②操作过程中,样品稀释不规范或均质时间过短会也会直接影响实验结果;③样品的存储和运输应该严格按照要求执行,否则可能到导致结果出现偏差;④样品冷冻后没有放置达到室温即开始实验,温度迅速升高导致菌体破裂受损,在规定的培养时间内菌体没有完全恢复,导致计数时菌数低[5];⑤VRBA作为一种选择性培养基,性能决定了检测结果质量的高低,还应加强关键培养基和试剂的性能验收。
为保障本次大肠菌群能力验证结果的准确性,本实验室采用多个稀释度和3M大肠菌群纸片对照等技术手段。3M大肠菌群测试片含有VRB培养剂(Violet Red Bile),一种冷水可溶性的凝胶剂和四唑翁(tetrazollium)指示剂,可增强菌落计数效果。表面覆盖的胶膜,可留住发酵乳糖的大肠菌群产生的气体。能力验证结果反馈表明,3M纸片法的检测结果更接近指定值,测试片的检测结果稳定可靠,且其具有快速简便的特点,可作为实验室检验的辅助手段和大批量食品微生物快速检测方法。在以后的能力验证考核中,还可加入基质辅助激光解吸/电离飞行时间质谱仪(MALEI-TOF-MS)等技术手段,对结果进行进一步确证,可以排除干扰菌,使检验结果更加准确。
参考文献
[1]刘云国.食品卫生微生物学标准鉴定图谱[M].北京:科学出版社,2009.
[2]许金榜.VRBA和3M PetrifilmTM快速测试片定量检测大肠菌群的性能比较研究[J].质量技术监督研究,2021,1(73):
17-22.
[3]中国合格评定国家认可委员会.能力验证规则:CNAS-RL02:2018[S].北京:中国标准出版社,2018.
[4]国家卫生和计划生育委员会,国家食品药品监督管理总局.食品安全国家标准 食品微生物学检验 大肠菌群计数:
GB 4789.3—2016[S].北京:中国标准出版社,2016.
[5]赵丽,申玉金,胡宝翠,等.多种不同方法对微生物能力验证样品测试结果的比较及分析[J].食品安全质量检测学报,2021,12(1):320-325.
热点推荐
-

“喂饱”体内的益生菌,肠道更健康
-

全十红红稗饼干|中秋团圆,回家必备
-

和汪氏蜂蜜共同来普及蜂蜜结晶现象
-

拿坡海开启西餐加盟新潮流, 大众化家庭小西餐成未来新趋势
-

摩购空间“霸王餐”来袭 打破传统营销套路带动商家业绩翻倍
-

食品中大肠菌群检测结果与分析
-
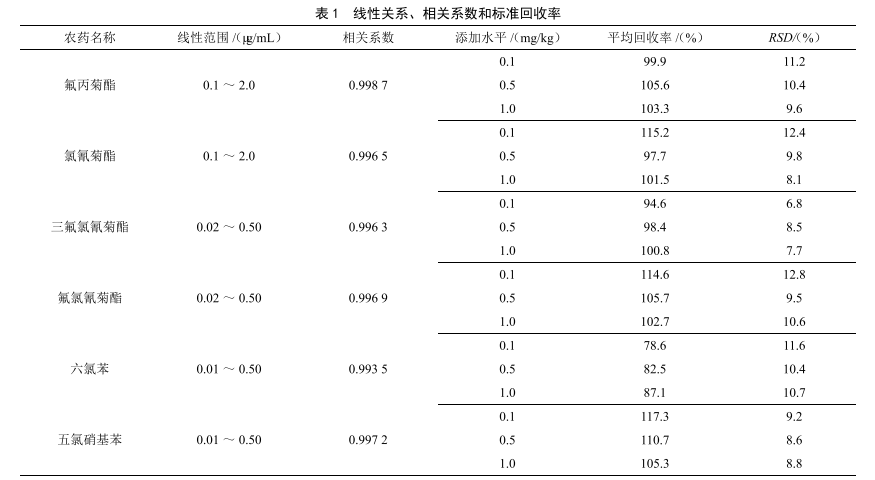
气相色谱法测定大米中多种农药残留量
-
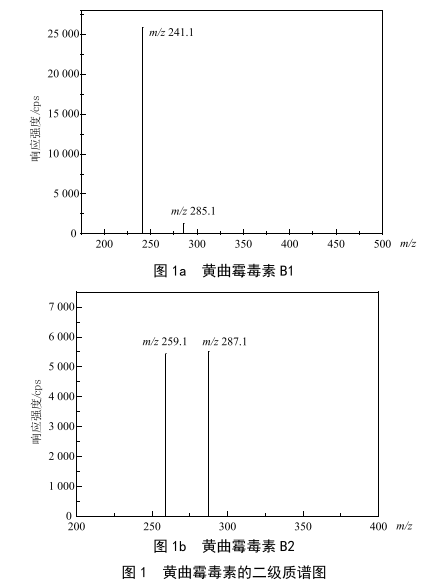
分散液液微萃取-超高效液相色谱-串联质谱法测定茶饮料中黄曲霉毒
-

辣椒及其制品中辣椒素含量检测及辣度分级
-
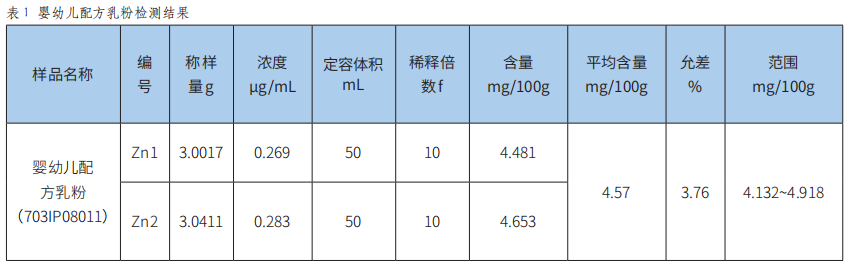
火焰原子吸收光谱法测定食品中锌的方法验证
-
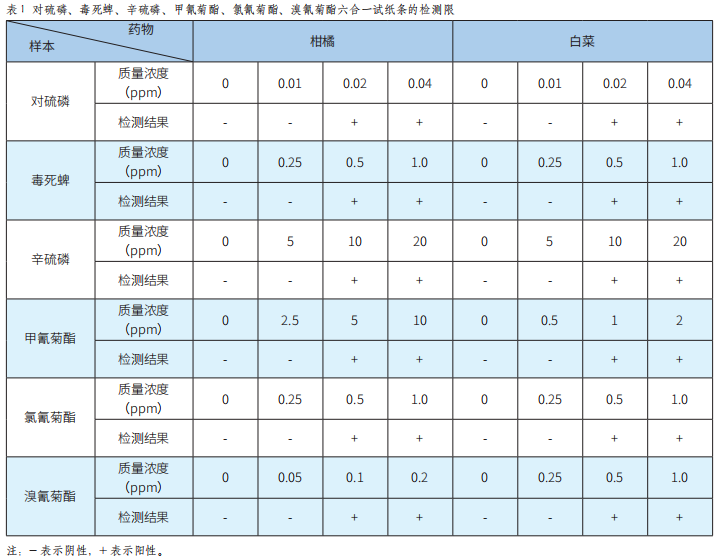
对硫磷等6种农药残留荧光免疫检测芯片的研发及应用
-

山东省潍坊市市售蔬菜中农药残留现况及慢性膳食暴露风险评估
-

食品检验检测机构质量控制的探讨
-
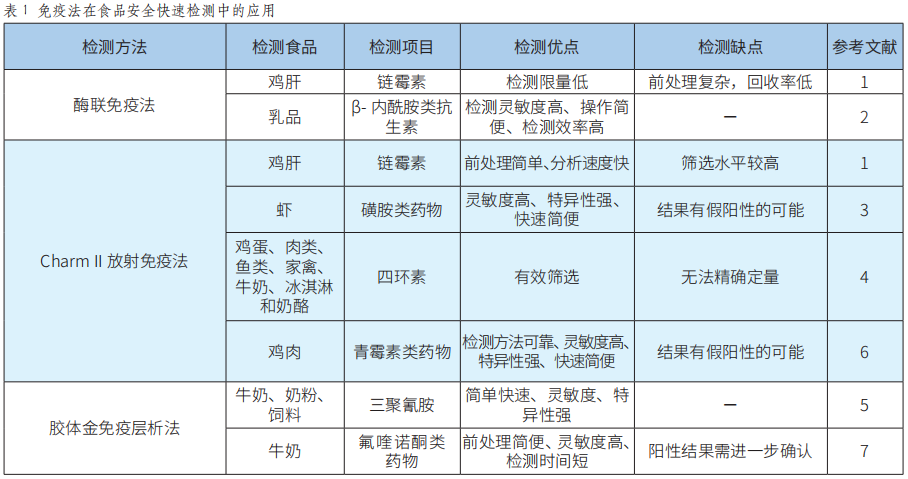
快速检测技术在食品安全中的应用研究进展
-
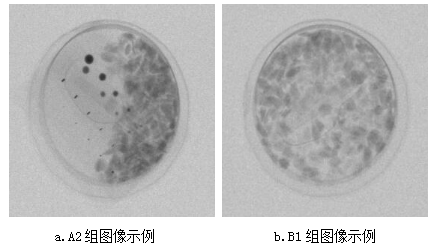
基于X射线图像的坚果盒异物检测
-
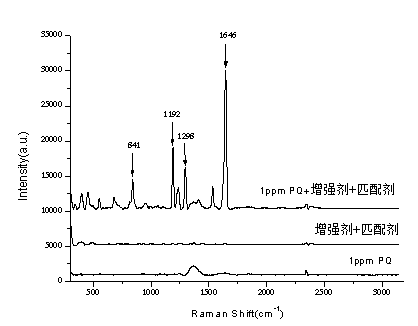
表面增强拉曼光谱法快速检测调味品中的百草枯
-
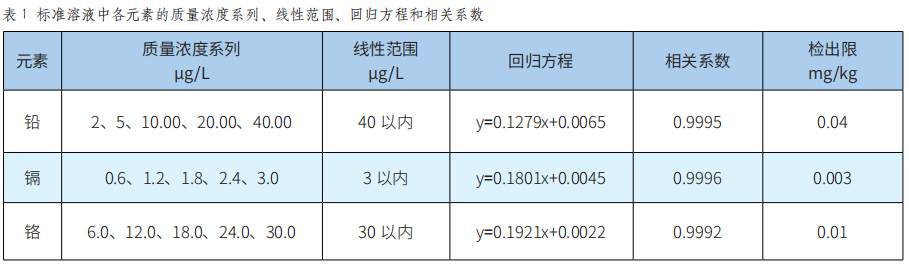
潞党参重金属污染物含量的评估
-
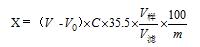
电位滴定法测定特殊医学用途食品中氯化物的不确定度评定
-
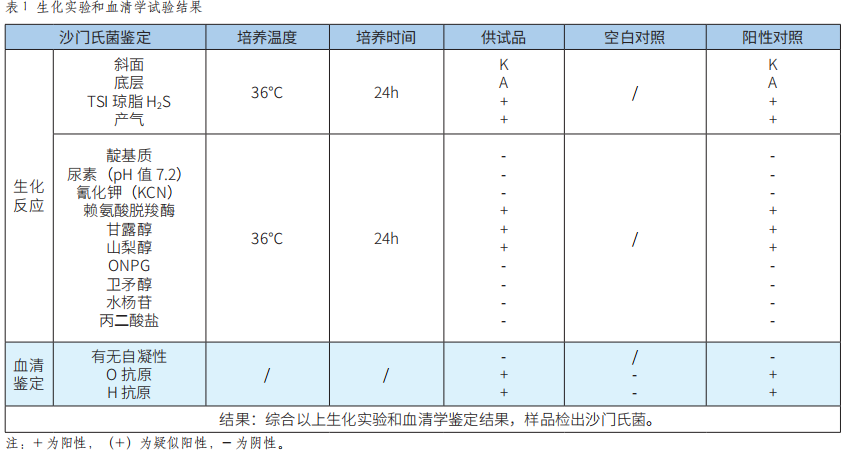
API 20E鉴定系统等两种检测方法应用于食品中沙门氏菌的检测结果
-

2020年上海市青浦区肉制品中单增李斯特菌分子分型及耐药性分析
-
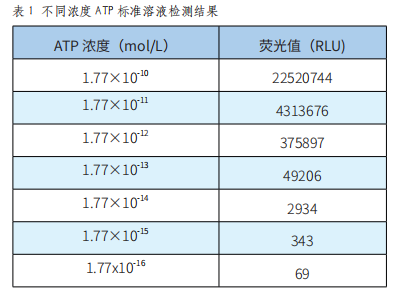
一种基于ATP荧光反应的洁净度检测系统的开发与验证
-
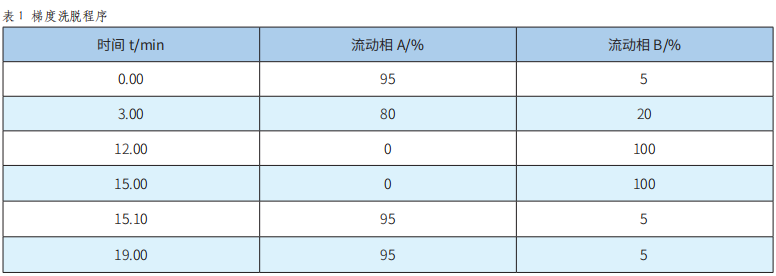
固相萃取-高效液相色谱-二极管阵列检测法测定饮料中9种人工合成着
-

一种检测盐霉素胶体金试纸条的研制及其应用
-

高效液相色谱法测定绿豆糕中5种常见的食品添加剂
-
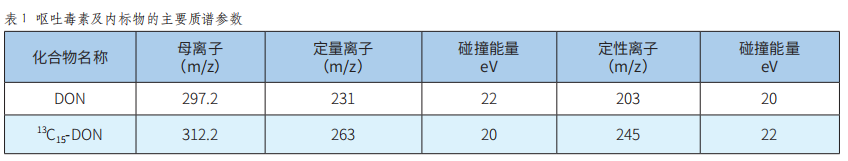
液相色谱-串联质谱内标法测定全麦粉中呕吐毒素含量的不确定度评
-
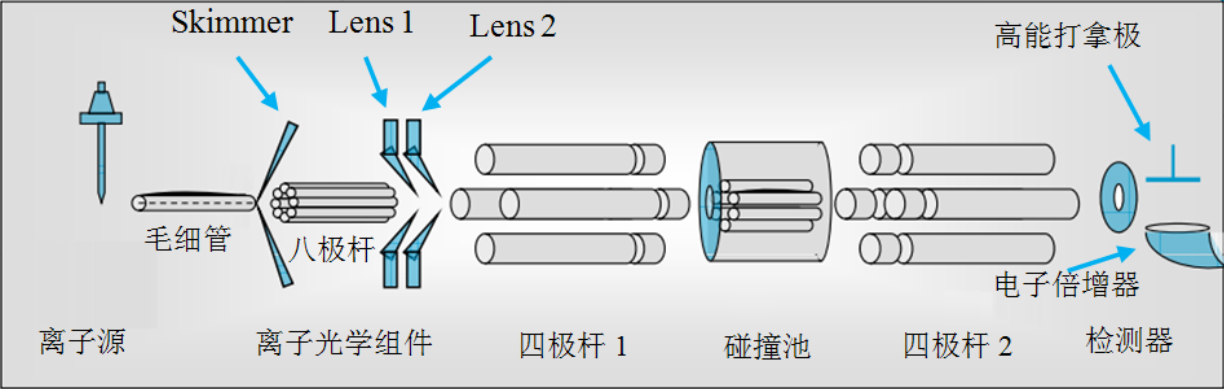
浅析QuEChERS方法结合色谱串联质谱技术在果蔬农药残留检测中的优势
-
食品检测技术问题及其解决措施研究
-
梅特勒-托利多最新版 ProdX™ 软件引入工业 4.0 功能
-
气相色谱-质谱法测定曼陀罗药酒中莨菪碱的含量
-

食品中鸡源性成分标准检测方法的比较性研究





