浅谈蛋白质含量的测定
2021-11-30 14:48:38 来源: 食品安全导刊
浅谈蛋白质含量的测定
张 琳,顾风云,秦宇婷,姜卓君,刘传玉
(吉林省产品质量监督检验院,吉林长春 130000)
摘 要:蛋白质是人体中非常重要的组成成分。蛋白质含量测定的常用方法有凯氏定氮法、双缩脲法、酚试剂法、紫外吸收法及燃烧法等。基于此,本文对蛋白质含量的测定进行了研究。
关键词:蛋白质;分析方法;凯氏定氮法
蛋白质是构成生命的重要物质[1]。在人体的细胞和组织中,蛋白质是非常重要的组成成分。在人体中,蛋白质占了人体质量的18%,其与生命现象有着密切的关系。人体内蛋白质的种类很多,但性质和功能各有区别。因此,蛋白质的检测方法就显得尤为重要。凯氏定氮法是测定蛋白质含量最为普遍的方法,同时相比较于其他检测方式,其具有更多优势[2],如易于操作、实验过程安全、成本较为合理、测定结果准确。因此,凯氏定氮法成为食品检验工作中普遍的测定方法。
1 实验仪器与试剂
实验仪器:电子天平(Metteler Toledo ML204);石墨消解仪(济南海能仪器股份有限公司);全自动凯氏定氮仪(山东海能科学仪器有限公司)。
试剂:硫酸铜;硫酸钾;硫酸;硼酸;氢氧化钠;甲基红指示剂;溴甲酚绿指示剂;95%乙醇溶液。
2 实验方法
2.1 实验原理
食品中的蛋白质在催化加热条件下被分解,产生的氨和硫酸结合生成硫酸铵。碱化蒸馏使氨游离,用硼酸吸收后以硫酸或者盐酸标准滴定溶液滴定,根据酸的消耗量计算氮含量。凯氏定氮法的反应过程包含以下几个方面。
消化:蛋白质+浓硫酸硫酸铵+二氧化碳+二氧化硫+水
蒸馏:氢氧化钠+硫酸铵→氨气+硫酸钠+水
吸收:氨气+硼酸→硼酸铵+水
滴定:硼酸铵+水+盐酸→氯化铵+硼酸
2.2 滴定注意事项
在滴定过程中需要注意以下两点。①指示剂为甲基红溴甲酚绿,其在碱性条件下变蓝,酸性条件下暗变红。②催化定氮片。硫酸铜催化剂;硫酸钾防止暴沸。
2.3 样品处理及实验步骤分析
①称量。固体试样0.2~2 g、半固体试样2~5 g,液体试样10~25 g。②消化。于消化管中加入硫酸铜、硫酸钾,10 mL浓硫酸后,放置石墨消解炉上消解90 min,消解温度为420 ℃,消解仪可选用曲线加热模式和直线加热模式。③上机。消解后的样品冷却后,可上机测试。上机测试前,需要对机器进行清洗,包括接受杯、碱管路,机器,清洗完毕后,先测试空白样品,再测试样品。④计算。根据公式可知,试样的质量、试剂空白滴定液体积、试样滴定液体积和氮换算为蛋白质的系数是变量,因此,实验过程中需要关注天平的准确性、消解是否完全、机器清洗是否干净、空白试剂的滴定体积数以及试验滴定液体积数是否准确。
3 仪器常规维护保养
①仪器要有良好的通风和散热条件。②仪器测试时首先进入清洗界面选择,换酸清洗3次左右,当改变滴定酸的浓度时,用换酸清洗的方法将管路及滴定器中的滴定酸排净,再用新换酸冲洗至少6次,并及时排液。③测样前连续做仪器空白测试[3]。等到仪器稳定后可测试样品(将机器中的碱量调为零,进行测试,当滴定体积之差小于0.05 mL,机器即为稳定)。④每日实验结束后,清洗接收杯1~2次以及碱管路2次,用洗瓶冲洗蒸馏头残余碱液。仪器前部的槽皿中,如果积有液体,将其擦洗干净。⑤为了延长防溅装置的使用寿命,请每天工作结束后清洗,即消化管内加入一半左右的蒸馏水(以蒸馏完成消化管液体不溢出为准),上机蒸馏,一般清洗2次左右(空蒸仪器把加碱量设置为“0”)。⑥仪器使用结束后要关闭水源、电源,仪器上要安装空消化管(防止防溅装置内残留液体流到仪器上)。⑦为防止碱路结晶影响仪器寿命,在完成实验后,进行碱管路清洗。若仪器长时间不用或者使用时间一周以上时,应将碱桶中的碱液换为蒸馏水;将消化管放好,选择手动加碱,达到清洗管路的作用,防结晶堵塞。⑧碱液桶、硼酸液桶应定期清理沉淀物并清洗干净。⑨仪器长期使用,在蒸馏瓶中会有水垢产生,将影响加热效率(建议6个月清理1次);如使用频繁,可增加清洗频率[4]。通过加蒸馏水管路加入除垢剂或一定浓度的弱酸性溶液清洗干净,按蒸馏水排水阀排净,再用蒸馏水多次冲洗后将管路连接好。⑩如仪器存放环境温度低于零度以下应排空仪器内所有液体,以免造成仪器损坏。
4 注意事项
①实验前,试剂要准备充足,保证满足本批次实验;②开机前要打开冷却循环水,保证冷却效果;③强酸强碱反应剧烈,建议设置加10~20 mL蒸馏水进行稀释;④添加氢氧化钾溶液的体积数为浓硫酸体积的4倍,最为适宜;⑤开始进行蒸馏时,消化管中液体的总体积以不超过总体积的1/3为宜;⑥拿取消化管的过程中需要注意高温烫伤。在放置消化管时,需要左右旋转几下,确保消化管与蒸馏头密封;⑦禁止使用边缘有缺口,或者有裂缝的消化管;⑧仪器蒸馏过程中如遇紧急情况,可直接关闭电源开关;⑨排废液管的出口要比仪器安放位置低,以使排液畅通。
5 实际应用与现状
在目前检测中,食品中蛋白质含量测试参照《食品安全国家标准 食品中蛋白质的测定》(GB 5009.5—2016)、《饲料中粗蛋白的测定 凯氏定氮法》(GB/T 6432—2018),同时,凯氏定氮仪还可以测定食品中挥发性盐基氮的含量,参照标准为GB 5009.228—2016以及测定大豆肽粉中多肽含量,参照标准为GB/T 22492—2008。凯氏定氮法测量蛋白质含量最为合适[5]。蛋白质的测定有凯氏定氮法、双缩脲法、酚试剂法、紫外吸收法和燃烧法,其具体操作及特点如下。
5.1 凯氏定氮法
准备4个50 mL凯氏烧瓶并标号,向1、2号烧瓶中加入定量的蛋白质样品,另外两个烧瓶作为对照,在每个烧瓶中加入硫酸钾-硫酸铜混合物,再加入浓硫酸,将4个烧瓶放到消化架上进行消化,之后进行蒸馏,全部蒸馏完毕后用标准盐酸滴定各烧瓶中收集的氨量,直至指示剂混合液由绿色变回淡紫红色,即为滴定终点,结算出蛋白质含量。
5.2 双缩脲法
双缩脲法是第一个用比色法测定蛋白质浓度的方法,硫铵不干扰显色,Cu2+与蛋白质的肽键以及酪氨酸残基络合,形成紫蓝色络合物,此络合物在540 nm波长处有最大吸收。首先利用标准蛋白溶液和双缩脲试剂绘制标准曲线,将待测血清与硫酸钠在待测试管中混合[6],并用只加入硫酸钠不含血清的试管作为对照,将两支试管加入等量的双缩脲试剂,充分混合后于37 ℃环境中放置10 min,在540 nm波长处进行比色,以对照管调零,读取吸光度值,由标准曲线上直接查出蛋白质含量。双缩脲法常用于0.5~10 g/L含量的蛋白质溶液测定。
5.3 酚试剂法
取6支试管分别标号,前5支试管分别加入不同浓度的标准蛋白溶液,最后一支试管加待测蛋白质溶液,不加标准蛋白溶液,每支试管液体总量通过加入蒸馏水补足而保持一致,将液体混合均匀,在室温下放置30 min,以未加蛋白质溶液的第一支试管作为空白对照,于650 nm波长处测定各管中溶液的吸光度值。
5.4 紫外吸收法
大多数蛋白质在280 nm波长处有特征的最大吸收,这是由于蛋白质中有酪氨酸,色氨酸和苯丙氨酸存在,可用于测定0.1~0.5 mg/mL含量的蛋白质溶液。取9支试管分别标号,前8支试管分别加入不同浓度的标准蛋白溶液,1号试管不加标准蛋白溶液,最后一支试管加待测蛋白质溶液[7],而不加标准蛋白溶液,每支试管液体总量通过加入蒸馏水补足而保持一致,将液体混合均匀[8],在280 nm波长处进行比色,记录吸光度值。
5.5 燃烧法
试样在900~1 200 ℃高温下燃烧,燃烧过程中产生混合气体,其中碳、硫等干扰气体和盐类被吸收管吸收,氮氧化物被全部还原成氮气,形成的氮气气流通过热导检测器进行检测。此方法易操作[9],但需要购买氮/蛋白质分析仪,采购费用比较昂贵。
参考文献
[1]张美娜.分光光度法在食品添加剂测定中的应用[J].粮食科技与经济,2018,43(9):54-56.
[2]曹坎涛.蛋白质测定方法改进[J].河北化工,2011,34(10):26-27.
[3]莫佳琳,张思原,陆海勤,等.钼酸铵分光光度法检测糖厂工业磷酸含量的应用研究[J].甘蔗糖业,2015(1):52-56.
[4]吴贺标,张顺红.分光光度法检测的应用及分析[J].啤酒科技,2001(10):51.
[5]李官慧.紫外-可见分光光度法在食品检测及食品安全分析中的应用[J].中国标准化,2017(22):72-73.
[6]李婷.分光光度法在食品检测中的应用标准研究[J].中国标准化,2017(16):57-58.
[7]郝丽红.分光光度法在食品检测中的应用标准研究[J].饮食科学,2017(14):12.
[8]汤亚芳.分光光度法在食品添加剂测定中的应用[J].广东化工,2016,43(10):209.
[9]董宇芳,潘临平.PAN萃取食品中锰的分光光度法的方法探讨[J].山西食品工业,1998(2):39-40.
热点推荐
-

使用梅特勒-托利多X光机的五大理由
-

小个头 大营养 禾泱泱有机稻鸭原生小泱胚芽米 金秋喜迎初丰收
-

全球食品创新平台第五期已启动,携手共创安全、健康、绿色的未来
-
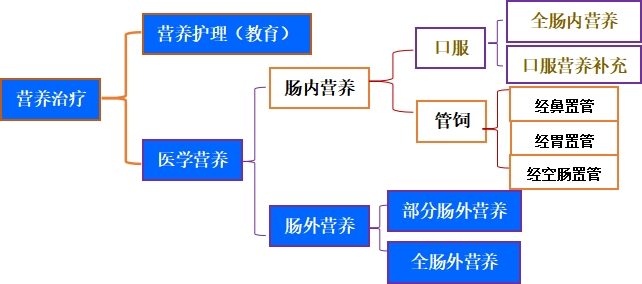
特医食品不是药,却是临床治疗的关键支撑
-

“喂饱”体内的益生菌,肠道更健康
-

武夷岩茶感官品质的审评
-

豆渣吸附刚果红的性能
-
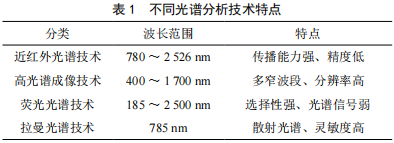
光谱和光谱成像技术在食品检测中的应用分析
-
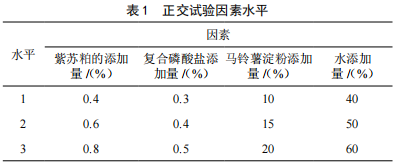
紫苏风味鸡肉丸加工工艺的研究
-
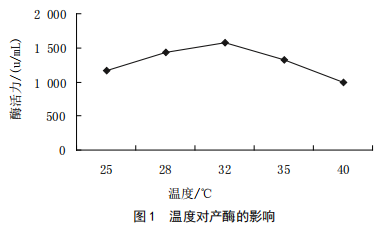
β-葡萄糖苷酶固体发酵培养条件的优化
-

青梅调味酱生产工艺及其功效研究
-
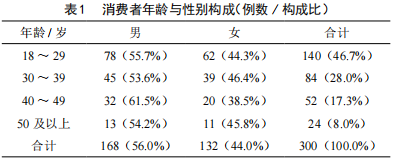
衡阳市城区消费者食品营养标签认知及影响因素分析
-
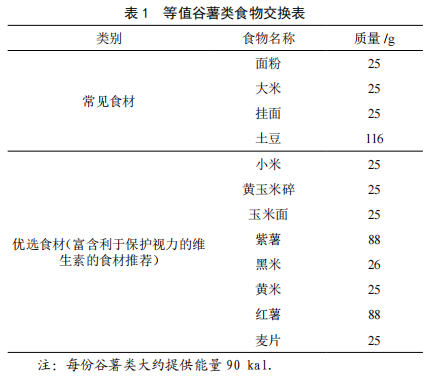
学龄儿童视力保护食谱设计与编制
-
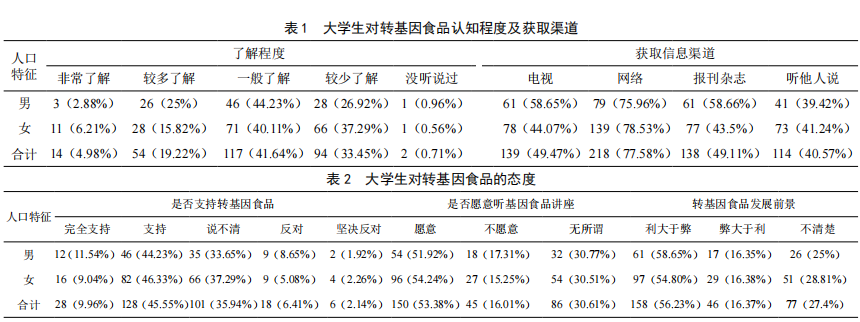
大学生对转基因食品的认知与态度探究——以石家庄市为例
-
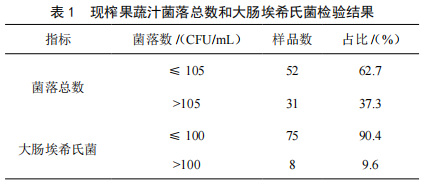
厦门市现制和自制饮品卫生状况调查与分析
-
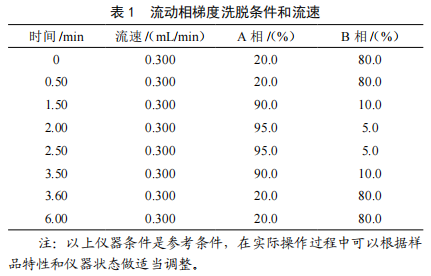
乳中地塞米松残留量检测方法的改进研究
-
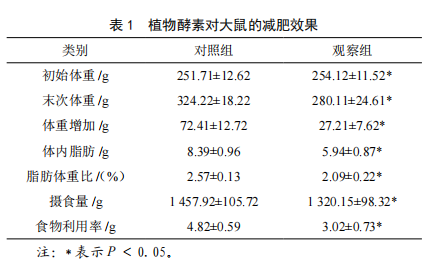
植物酵素发酵过程中几种功效酶的动态变化及减肥功效评价
-
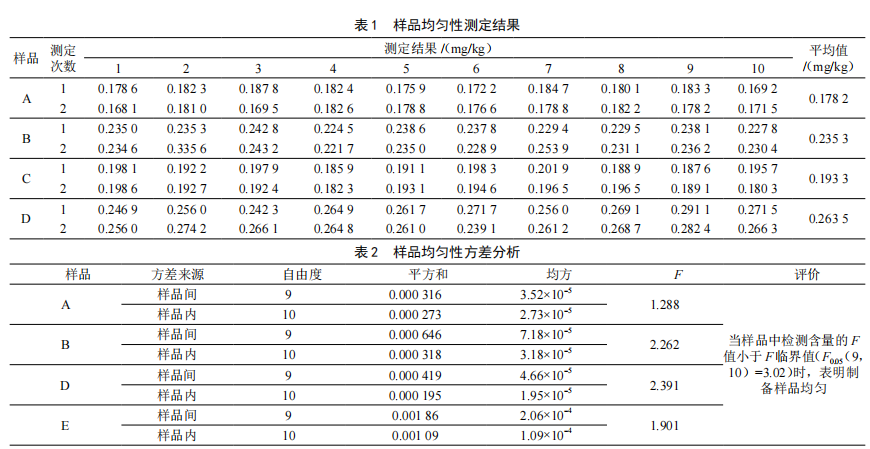
饮料中铅含量的测定能力验证样品的稳定性和均匀性分析
-
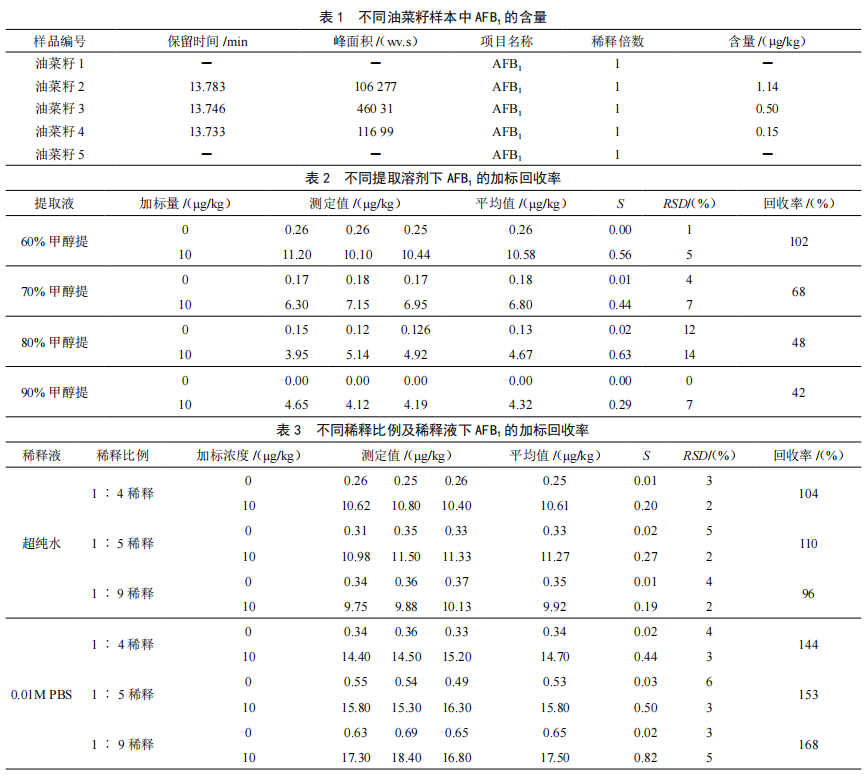
ELISA法检测油菜籽中的黄曲霉毒素B1
-
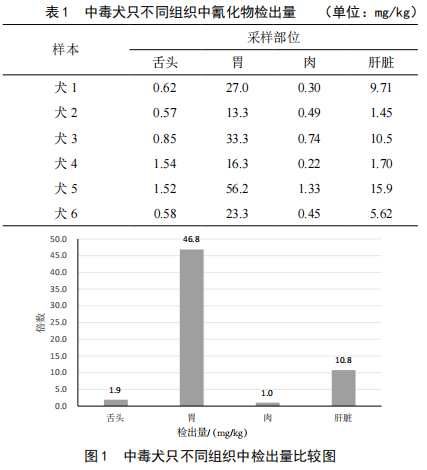
氰化物中毒犬只样品采样要点
-
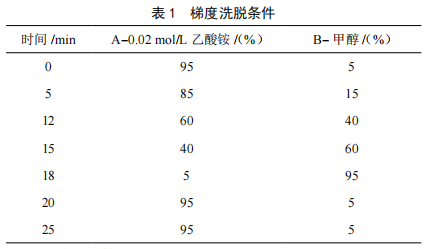
高效液相色谱法同时测定果酱中6种合成着色剂
-
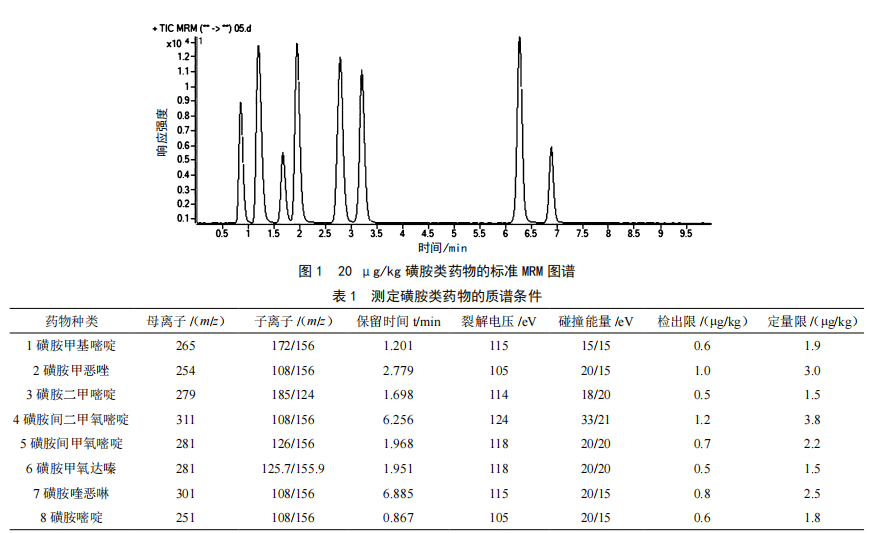
超高相液相色谱-串联质谱法测定鲜猪肉中8种磺胺类药物残留
-

基于漫反射红外光谱法的粮食真菌毒素检验方法
-

顶空-气相色谱法快速测定冰淇淋中环氧乙烷残留量
-
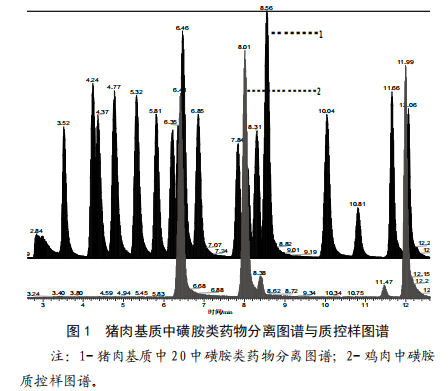
超高效液相色谱-串联质谱法测定动物源性食品中20种磺胺类药物残留
-
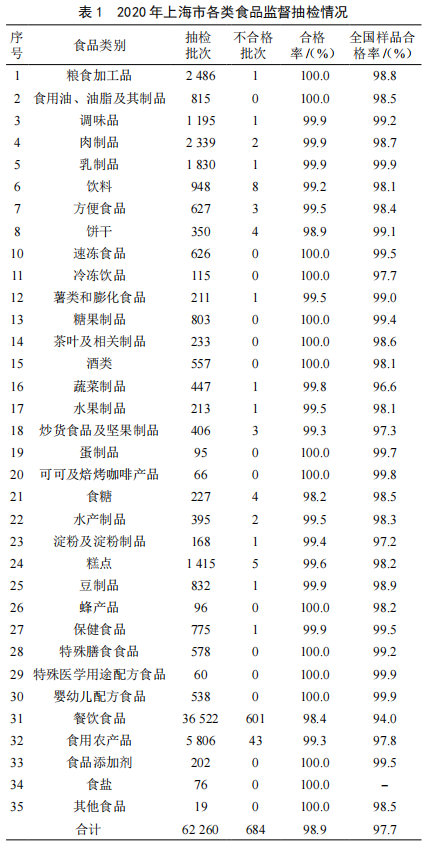
2020年上海市食用农产品监督抽检情况分析
-
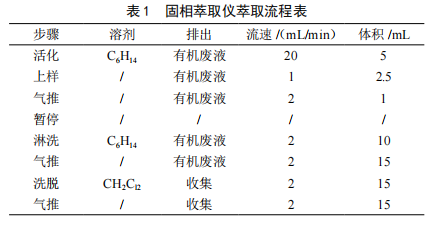
GC-MS检测白酒中氨基甲酸乙酯方法的优化
-
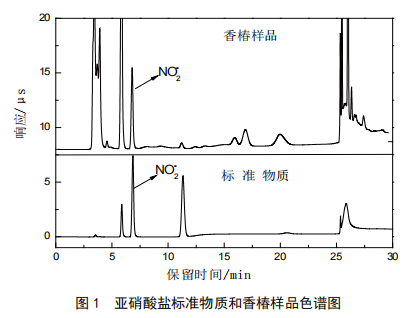
存储条件对香椿中亚硝酸盐含量检测的影响
-
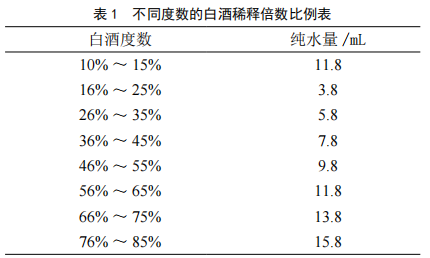
白酒中甲醇含量的便携式仪器快速检测法
-
超高效液相色谱测定饮料中的食品添加剂





