肉猪体内组织和体液中多西环素含量的相关性研究
2021-10-14 11:26:12 来源: 食品安全导刊
肉猪体内组织和体液中多西环素含量的相关性研究
余军军1,2,蓝棋浩1,2,宁 军1,2,韦 田1,2,梁立杰3,孙 坚3
(1.温氏食品集团股份有限公司,广东新兴 527400;2.广东省畜禽健康养殖与环境控制企业重点实验室,
广东新兴 527400;3.华南农业大学兽医学院,广东广州 510642)
基金项目:2019年广东省乡村振兴战略专项资金项目(2019B020401)。
作者简介:余军军(1986—),男,河南信阳人,硕士,兽医师。研究方向:兽用药物代谢动力学与残留检测技术。
摘 要:采用液相色谱串联质谱分析法,对肉猪体内组织(肌肉、肝脏、肾脏、肺脏)和体液(尿液、血液)中多西环素含量进行检测,分析多西环素在猪体内组织和体液中的残留消除情况,探讨多西环素在体液与各组织残留量的相关性,并预测达到休药期时体液中多西环素的含量范围。结果表明,猪混饮多西环素后各组织中药物代谢快,体液中药物浓度低,休药期为11 d,体液与各组织间药物残留量呈较高相关性。当尿液多西环素含量低于57.07 μg/L、血液低于2.76 μg/L时,预测99%动物体内组织中多西环素残留量低于最大残留限量,为肉猪宰前监测体内多西环素残留提供了一种简单经济的方法。
关键词:多西环素;猪;残留消除;休药期;宰前监测
多西环素(Doxycycline,DOX)是由土霉素在6-位脱氧而制成的第二代半四环素衍生物,又名强力霉素或脱氧土霉素,由美国辉瑞制药厂在上世纪60年代发明[1]。多西环素是广谱抗生素,对肠球菌、肺炎球菌、沙门氏菌、大肠杆菌、金黄色葡萄球菌、衣原体、支原体和立克次氏体等具有良好的抗菌效果[2]。因其在体内具有分布广、长效、高生物利用度和无明显肾毒性等特点,临床上广泛应用于猪、牛、鸡和羊的养殖,以治疗呼吸道、消化道和泌尿道的细菌性疾病。随着多西环素在兽医临床上的使用,其残留问题也越来越被重视。目前,国内外对多西环素在动物体内的残留消除的研究已有很多,但对多西环素在体内的残留监控主要用动物的可食用组织,尿液和血液中多西环素残留的消除及残留监控较少[3-4]。本文通过计算多西环素在猪体内的休药期,并预测休药期猪尿液和血液中药物残留量范围,以探索尿液或血液样品用于多西环素残留监控的可操作性。
1 材料与方法
1.1 材料
1.1.1 仪器设备
液质联用仪(QTRAP 5500,美国AB SCIEX公司);组织匀浆机(HM6300,北京Lab Precition公司);氮吹仪(MV5,北京莱伯泰科公司);电子分析天平(BT125D,德国Sartorius公司);冷冻高速离心机(5804R,德国Eppendorf公司);C18固相吸附剂(月旭科技公司);6cc/200 mg的固相萃取小柱(Oasis HLB,美国Waters公司)。
1.1.2 试剂
多西环素对照品,纯度97.2%,批号1-F-4F4-1,美国CATO公司;多西环素-D3对照品,纯度97%,批号T291402,加拿大TRC公司;甲醇、乙腈和甲酸均为色谱纯,购于德国默克公司;正己烷、三氯乙酸为分析纯,购于广州化学试剂厂;盐酸多西环素可溶性粉,兽药字190172193,含量10%,批号20191004,购于河北远征禾木药业有限公司。
1.1.3 试验动物的饲养与管理
选择健康、体重相近的三元杂商品猪41头(40.5±3.8) kg,随机分成2组,分别为对照组1头,试验组40头。试验组在基础饮水中添加盐酸多西环素可溶性粉,制成多西环素浓度为50 mg/L的药液,连续混饮给药5 d。于停药后第1 d、2 d、3 d、5 d、8 d、12 d、15 d和18 d随机选择5头猪只,采集组织(肌肉、肝脏、肾脏、肺脏)和体液(尿液、血液)作为检测
样品。
1.2 试验方法
1.2.1 溶液配制
(1)多西环素储备液(1 000 μg/mL).准确称取50.0 mg多西环素对照品,置于50 mL容量瓶中,用甲醇溶解并定容至刻度,摇匀密封,置-20 ℃冰箱中保存。
(2)多西环素-D3储备液(100 μg/mL)。准确称取1.0 mg多西环素-D3对照品,置于10 mL容量瓶中,用甲醇溶解并定容至刻度,摇匀密封,置-20 ℃冰箱中保存。
(3)三氯乙酸(1 mol/L)。准确称取16.3 g三氯乙酸置于100 mL容量瓶中,加入超纯水溶解并定容至刻度,摇匀。
1.2.2 样品处理
(1)组织。称取2.0 g匀浆后的组织样品置于50 mL离心管中,加入50 μL内标溶液(浓度5 μg/mL),静置
5 min。然后加入2 mL水、8 mL乙腈。涡旋混匀后,超声提取10 min。然后室温条件下4 000 r/min离心5 min,上清液倒入50 mL离心管中,加入500 mg C18吸附剂,涡旋30 s
净化。再重复离心1次,移取5 mL上清液在50 ℃水浴中氮气吹干。残渣中加入1 mL甲醇水(10︰90)、2 mL正己烷,涡旋30 s。室温条件4 000 r/min下离心10 min,吸取下层过0.22 μm滤膜,待测。
(2)尿液:取5 mL尿液样品于15 mL离心管中,并加入20 μL内标溶液(浓度5 μg/mL),静置10 min。将HLB萃取小柱固定在固相萃取装置上,依次用5 mL甲醇、5 mL超纯水活化后,倒入尿液样品,用5 mL水、5 mL甲醇水(20︰80)淋洗,抽干,5 mL甲醇洗脱,收集洗脱液。洗脱液在在50 ℃水浴中氮气吹干,残渣用1 mL甲醇水(10︰90)溶解,涡旋30 s。样品过0.22 μm滤膜,待测。
(3)血液。准确吸取500 μL血浆,依次加入20 μL内标(5 μg/mL)、500 μL三氯乙酸溶液,涡旋混匀,10 000 r/min室温条件下离心10 min,上清液过0.22 μm针头滤膜,待
上机。
1.2.3 仪器条件
(1)色谱条件:Waters Acquity UPLC BEH C18色谱柱
(2.1 mm ×50 mm,1.7 μm);流速:0.25 mL/min;流动相:A为0.1%甲酸溶液,B为甲醇;梯度洗脱条件:0~2 min,
5%~15% B;2~5 min,15%~40% B;5~7 min,40%~95% B;7~7.1 min,95%~5% B;7.1~12 min,5%。柱温为35 ℃。进样体积为10 μL。
(2)质谱条件:电喷雾离子源(ESI);多反应监测(MRM)正离子模式;离子源温度550 ℃;电喷雾电压(IS)5.5 kV;气帘气压力(CUR)、雾化气压力(GS1)及辅助气压力(GS2)分别为35 kPa、55 kPa和60 kPa。药物优化的去簇电压和碰撞能量等质谱参数见表1。
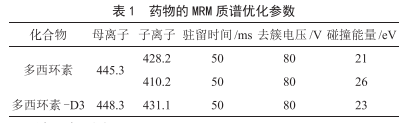
2 结果与分析
2.1 组织中多西环素残留消除规律
不同时间点各组织中多西环素残留量见表2。结果显示,10%多西环素可溶性粉按推荐剂量连续用药5 d后,多西环素在肝脏和肾脏中的残留含量最高,在肌肉、肺脏中的含量较低,停药2 d后,多西环素在肌肉和肝脏的残留量分别为(99.30±33.84)μg/kg和(104.51±29.20)μg/kg,均低于最高残留量MRL[5](肝脏300 μg/kg,肌肉100 μg/kg),停药3 d后,肾脏中的多西环素残留量为(350.28±136.12)μg/kg,低于了最高残留量MRL(肾脏600 μg/kg)。多西环素主要残留部位在肾脏,各组织中残留消除的速度较快,在停药后5 d,组织中均检测不出多西环素。在停药8 d采集的5头猪血液中,只有1份样品检出多西环素。
2.2 休药期计算
按照农业部对多西环素最大残留限量[5]和欧盟对休药期计算方法,利用WT1.4软件按双单侧99%置信区间计算多西环素在猪组织中休药期[6]。由图1可知,多西环素在肌肉中的休药期为10.58 d、肝脏为10.80 d、肾脏为8.13d、肺脏为10.51 d,考虑到给药方式等因素的影响,建议休药期为11 d。
2.3 体液中多西环素残留量相关性研究
通过统计学软件SPSS,采用统计学软件SPSS,对双变量“停药后体液中多西环素含量”“各组织中多西环素含量”进行相关性分析。由表3可知,停药后体液中多西环素残留量与各组织中多西环素残留量之间的相关系数大于0.85,相关系数的显著性水平为0.01,体液与各组织中多西环素残留量之间是高度相关的。



2.4 组织中药物残留量低于MRL时体液中残留量区间预测
使用SPSS软件对时间-体液中药物浓度进行线性分析,并根据建立的模型预测停药为10.80 d时的体液中药物浓度区间范围。结果显示,当时间为10.80 d时,即肉猪体内组织中多西环素残留量低于最大残留限量时,尿液中药物浓度区间范围为57.07~252.12 μg/L;血液中药物浓度区间范围为2.76~28.68 μg/L。


3 结论与讨
目前,常用的动物体内药物残留检测方法包括微生物法、毛细管电泳法、酶联免疫法、液相色谱法和液相色谱串联质谱法等,其中液相色谱串联质谱法作为唯一确证方法应用最多。庞国芳等[7]采用液相色谱串联质谱法检测了体内各组织和体液中多西环素的残留量,制定了该产品的休药期为11 d,为药物的临床使用提供了数据支持。
刘欣[3]按体重10 mg/kg的剂量给予盐酸多西环素颗粒,每天1次,连续5 d,研究多西环素在动物体内的消除规律,结果显示,停药后第3天,除1头猪肝脏组织中的残留量高于MRL外,其他各组织中药物的残留量均低于MRL,同时计算休药期为12 d[8-9]。而本试验结果中,停药后第3天,猪各组织中药物残留量均低于MRL,计算休药期为11 d,翟克影[4]也做了相关研究,除了剂型和给药方式不同,盐酸多西环素在猪体残留分布与消除结果基本相似。
在实际生产中,通过对猪活体尿液样品的检测,建立的回归方程,可以间接判断猪体内多西环素残留量是否低于最大残留限量。20世纪末开始已有不少学者采用这种经典回归法来预测组织中药物的残留浓度,但在研究时均没有考虑个体间差异,试验的重复性较差[10]。本文根据停药后尿液、血液中药物消除情况,引入置信区间预测,考虑了个体间差异,通过计算发现当动物停药时间到达休药期时,尿液中多西环素残留量区间下限为57.07 μg/L、血液为2.76 μg/L,表明可通过监测体液中多西环素浓度判断动物体内组织中药物残留量是否安全。考虑到尿液样品获取更便捷,采取时动物应激更小,动物屠宰前可检测尿液判断动物是否符合屠宰要求,判定限为57 μg/L。
参考文献
[1]赵婵娟.多西环素研究进展[J].湖北畜牧兽医,2012(12):
10-14.
[2]操继跃.猪呼吸系统感染性疾病药物治疗[J].养殖与饲料,2005(4):39-43.
[3]刘欣,魏丽娟,瞿红颖,等.盐酸多西环素颗粒在猪体内残留消除的研究[J].黑龙江畜牧兽医,2017,539(23):201-203.
[4]翟克影.盐酸多西环素可溶性粉在猪体内药物动力学及残留研究[D].武汉:华中农业大学,2008.
[5]中华人民共和国农业农村部,国家卫生健康委员会,国家市场监督管理总局.食品安全国家标准 食品中兽药最大残留限量:GB 31650—2019[S].北京:中国标准出版社,2019.
[6]Nahler M.Committee for veterinary medicinal products (CVMP)[J].Springer Vienna,2009,296:9-10.
[7]庞国芳.兽药多组分残留分析技术[M].北京:科学出版社,2016.
[8]Chiesa L,Nobile M,Arioli F,et al.Determination of veterinary antibiotics in bovine urine by liquid chromatography-tandem mass spectrometry[J]. Food Chemistry,2015,185(15):7-15.
[9]Junior L B,Leal M G,Uchoa F,et al.Determination of quinine and doxycycline in rat plasma by LC–MS–MS:Application to a pharmacokinetic study[J].Chromatographia,2011,73(11):1081-1088.
[10]黄显会,蔡勤仁,刘戎,等.克伦特罗在猪组织和尿液中残留消除规律研究[J].动物毒物学,2003,18(1):32-37.
热点推荐
-

主要食品配料厂商携手支持可持续农业
-

别样肉客在华推出脆香酥炸植物基蟹饼,为新春佳节增添美食新选
-

ADM首度亮相FBIF2023,探索食品饮料的今天、明天和未来
-

专访婴儿水团体标准制定者:为何为婴儿饮用水制定更高标准?
-

使用梅特勒-托利多X光机的五大理由
-

广西发动全区3·15食品安全“你点我检 服务惠民生”问卷调查
-

河南全省食品安全监管工作会议在鹤壁召开
-

万里挑一的“进博TOP好物”,三养创新产品与食安承诺受赞誉
-

河南省餐饮食品安全“总监话总监”巡讲活动在洛阳启动
-

郑州市举办2024年“质量月”质量诚信进商超暨质量提升交流观摩会
-

仁和中方医药股份联合民生大药房送健康捐赠活动在郑州举行
-

三养密阳工厂深度揭秘:火鸡面的食品安全与品质卓越之道
-

郑州市金水区召开学校食堂承包经营企业 食品安全行政指导会
-

陕西省举办全省学校食堂食品安全管理及投诉处置现场会
-

山西省局举办质量提升行动助力汾酒专业镇高质量发展活动
-

郑州市金水区开展肉类产品质量安全专项整治
-

郑州市市场监管局开展网络餐饮服务食品安全行政指导工作
-

西藏山南市率先将“两个责任”进党校 推动食品安全社会共治
-

湖北:开展校园食品安全和“五一” 期间食品安全监管工作
-

河南省政府食品安全办召开2024年夏季食品安全形势会商会议
-

山西省局召开食品安全抽检承检机构任务部署会
-

南昌市开展春节前食品经营安全监督检查
-

河南省汝南县:“你点我检服务惠民生”护航“双节”食品安全
-

湖北省局推动共建“外卖小哥食堂” 让外卖骑手暖心又暖胃
-

焦作市校园食品安全排查整治专项行动动员部署会召开
-

汝南县市场监管局“四个抓手”提升集中用餐单位食品安全水平
-

山西省市场监管局食品案件查办指导中心正式挂牌运行
-

河南省汝南县市场监管局多措并举开展学校食堂食品安全评价
-

恩施州市场监管局服务第八届世界硒博会
-

开封市市场监管局2023年食品抽检工作质量提升推进会召开





