湿式大肠菌群快检纸片性能验证的方法探索
2021-08-30 14:51:57 来源: 食品安全导刊
湿式大肠菌群快检纸片性能验证的方法探索
刘 哲,李丹妮,王 宇,王 涛,王 萌,冯 淑
(延安市食品质量安全检验检测中心,陕西延安 716000)
作者简介:刘哲(1989—),男,汉族,陕西延安人,本科,助理工程师。研究方向:食品检验。
摘 要:目的:探索对市售湿式大肠菌群快检纸片性能进行分析、验证的一般流程,为检测、监测机构、企业和个人选用、验收该类快检产品提供参考。方法:从纸片的污染指标、特异性指标、检出水平(LODX)、检测结果有效性和产品质量稳定性等方面进行试验研究,对纸片的性能进行综合分析和验证。结果:纸片的各项试验结果基本符合预期和产品自身的质量要求。结论:本文所探索的对湿式大肠菌群快检纸片性能进行分析验证的一般流程可有效对该类纸片产品进行较为全面的性能验证,在使用该类快检产品时可作为产品选用和验收、验证的参考。
关键词:大肠菌群;快检纸片;性能验证
大肠菌群是指一类在一定培养条件下能够发酵乳糖、产酸产气的需氧或兼性厌氧革兰氏阴性无芽孢杆菌[1]。湿式大肠菌群快检纸片是近年来新出现的可用于餐(饮)具或公共场所用品用具大肠菌群检测的快检产品,该类产品具有携带方便、操作简单等特点,且相较于干式快检纸片省去了使用无菌生理盐水润湿纸片的环节,从而降低了检测操作和环境污染的风险[2]。
近年来,随着各类快检产品出现的越来越多,各产品的质量也参差不齐[3-4],产品使用单位或个人对所购买产品的性能缺乏有效了解。本文将着重探索对湿式大肠菌群快检纸片的性能进行分析、验证的一般流程,为产品使用单位或个人选用和验收、验证该类大肠菌群快检产品提供参考。
1 材料和方法
1.1 材料与试剂
环境样本(自然环境、居住、办公环境等)、人工污染样本。湿式大肠菌群快检纸片、月桂基硫酸盐胰蛋白胨肉汤(LST)、煌绿乳糖胆盐肉汤(BGLB)、营养肉汤(NB)、营养琼脂(NA)、无菌接种环、无菌移液管、无菌平皿等。
标准菌株:大肠埃希氏菌(ATCC 25922)、弗氏柠檬酸杆菌(ATCC 43864)、产气肠杆菌(ATCC 13048)、福氏志贺氏菌(CICC 21534)、鼠伤寒沙门氏菌(ATCC 14028)、粪肠球菌(ATCC 29212)和金黄色葡萄球菌(ATCC 6538)。
1.2 仪器与设备
生物安全柜、冰箱(2~8 ℃)、培养箱(36±1)℃、涡旋振荡器、移液枪等。
1.3 方法
本文将着重对纸片的污染指标、特异性指标、检出水平(LODX)、检测结果有效性和产品质量稳定性验证等方面进行试验分析。
1.3.1 污染指标
选取2~4个不同批号(本次试验为4个批号:200605、200903、210505和210506)的湿式大肠菌群快检纸片产品,无菌操作,每个批号分别取5张快检纸片,装入纸片配套的无菌小袋中,置(36±1)℃培养箱中培养18 h,观察结果。
1.3.2 特异性指标
本文综合湿式大肠菌群快检纸片自身的产品质量要求和《食品安全国家标准 食品微生物学检验 培养基和试剂的质量要求》(GB 4789.28—2013)中对大肠菌群相关培养基、试剂的质量要求,确定使用大肠埃希氏菌、弗氏柠檬酸杆菌、产气肠杆菌、福氏志贺氏菌、鼠伤寒沙门氏菌、粪肠球菌和金黄色葡萄球菌等7种菌对纸片进行大肠菌群的特异性验证。
验证时,用无菌接种环从上述7种菌的新鲜营养琼脂斜面上沾取一环菌,直接于纸片表面划线,然后置于(36±1)℃培养箱中培养18 h,观察各菌在纸片上的特异形态。本文试验中选取了4个不同批号(同1.3.1)的纸片进行特异性验证。
1.3.3 检出水平(LODX)
本文通过纸片对高、中、低3个接种水平和空白的样本匀液的测试结果来获得该纸片法的检出水平(由于测试的样品数量较少,本文中使用“估计LOD50”[5]),高、中、低3个接种水平和空白分别做2个测试,共获得8个结果。记录每个接种水平获得的阳性结果(检出)数量,使用《微生物检测方法确认与验证指南》(RB/T 033—2020)附录B中的表B.1确定估计LOD50。
高水平接种量为不超过预期LOD50(预期的LOD50设定为:≤3 CFU/测试单元[5])的10倍,中水平接种量可由高水平接种物稀释2倍获得,低水平接种量可由高水平接种物稀释10倍获得。
用大肠埃希氏菌(ATCC 25922)制备浓度(单位:CFU/mL)分别为高、中、低接种水平10倍的接种物匀液。测试时,无菌操作,先取适量湿式大肠菌群快检纸片置于配套的无菌袋中,然后分别吸取0.1 mL(测试单元)各接种水平的接种物匀液和空白液,均匀滴加(接种)于纸片表面,每个接种水平和空白分别测试2张纸片,滴加(接种)完成后,将纸片置于(36±1)℃培养箱中培养18 h,观察结果。同时,分别吸取0.1 mL各水平接种物匀液和空白液加入2个无菌平皿,立即倒入15~20 mL冷却至46 ℃的营养琼脂,摇匀,(36±1)℃培养24 h,计数,对各接种水平的接种物匀液浓度和空白对照进行同步确认。观察并记录测试结果。
1.3.4 检测结果有效性
本文试验中,为覆盖更广泛的微生物种类,用湿式大肠菌群快检纸片对采集的21个自然环境(土壤、河流、小溪等)样本、30个居住环境(厨房、餐厅、卫生间和卧室等)样本和20个办公环境(办公室、走廊、电梯间、公共卫生间等)样本,共计71个环境微生物样本进行检测,然后将所有的检测结果用《食品安全国家标准 消毒餐(饮)具》(GB 14934—2016)中的附录B B.1发酵法进行确认,从而对纸片的检测结果有效性进行验证。
操作时,环境表面的微生物样本直接用纸片进行采集,土壤、河流等不适合直接采集微生物的样本,加无菌生理盐水振荡提取其中的微生物后,取适量提取液置营养肉汤(NB)中培养过夜,再取样本培养液划线接种于纸片,(36±1)℃培养18 h,记录检测结果。液体样本直接取适量样本匀液经肉汤增菌后,取增菌液划线接种于纸片。
无菌操作,将培养后的纸片全部分别转移至LST肉汤管,置培养箱中(36±1)℃培养24~48 h,进行发酵试验。后续复发酵试验和结果判定按GB 14934—2016附录B B.1发酵法中的要求进行。观察并记录测试结果。
1.3.5 产品质量稳定性
同一生产批号的纸片可通过在常规条件下保存3~6个月以上后再次进行污染指标和特异性指标的验证来分析该纸片在产品有效期内的质量稳定性,本次试验选取已于常规保存条件下保存11个月的湿式大肠菌群快检纸片(生产批号:200605)进行验证。不同生产批号纸片质量的持续稳定性由1.3.1~1.3.3的试验中,同时或先后选取2~4个不同批号的纸片进行验证。
2 结果与分析
2.1 污染指标
试验中4个不同批号的纸片经(36±1)℃培养18 h后,均无变化,保持初始的状态和颜色(湿润、平整,紫色)。表明在无菌操作及规定的培养条件下,纸片和配套的无菌塑料小袋自身不会出现污染而干扰大肠菌群检测。
2.2 特异性指标
试验结果显示,3种大肠菌群(大肠埃希氏菌、弗氏柠檬酸杆菌和产气肠杆菌)在纸片上生长旺盛,且呈现典型的阳性反应,即纸片上可见点、线状红色斑点或片状红晕,斑点周围变黄或明显变黄。其他4种菌中,鼠伤寒沙门氏菌和福氏志贺氏菌呈阴性反应,即纸片上可见点、线状红色斑点或片状红晕,但斑点或红晕周围颜色不变。另外2种革兰氏阳性菌处于被抑制状态,只可见少量红色斑点或红晕且斑点或红晕周围不变色,呈阴性反应,且各菌在不同批号纸片上的特异形态无明显区别。说明本次试验中该纸片对大肠菌群和非大肠菌群细菌可呈现明显的特异性反应,且对革兰氏阳性菌有一定抑制作用。
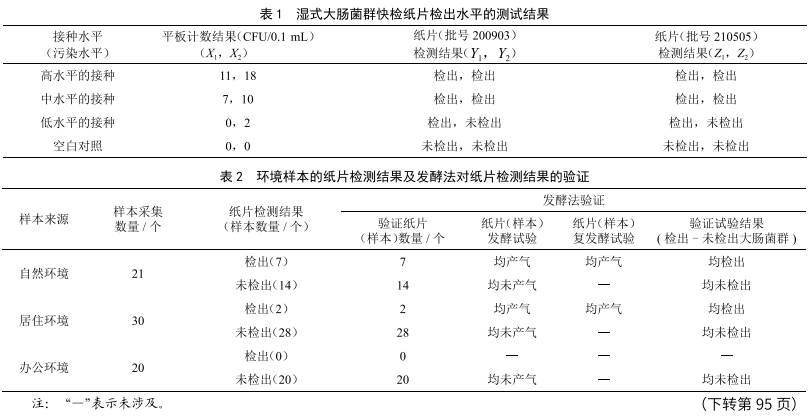
2.3 检出水平(LODX)
检出水平的测试结果见表1。结果表明,纸片在样品(接种物匀液)处于低污染水平时,即测试单元(0.1 mL样液)中的目标微生物数为1CFU((0+2)/2=1)时,即有50%的概率检出该菌(2张测试纸片中有1张检出(阳性))。在高污染水平和中污染水平时2张纸片均检出。且2个批号的纸片测试结果一致。查RB/T 033—2020附录B 表B.1,得估计LOD50(CFU/测试单元)=1 CFU/测试单元。测试结果间接表明该纸片的性能符合预期。
2.4 检测结果有效性
样本的纸片检测结果及发酵法对纸片检测结果的验证见表2。结果表明,在本次试验中,该纸片的检测结果与发酵法的验证结果一致,说明对采集到的同一样本,其与发酵法的检测结果一致,表明该纸片显示的检测结果与发酵法结果同等可靠有效。

2.5 产品质量稳定性
同一批号(200605)的纸片在常规条件下保存11个月之后,其污染指标和特异性指标试验结果未发生变化。不同批号的纸片,其污染指标、特异性指标和检出水平的测试结果一致(参见2.1~2.3)。
结果表明该纸片不论是同一批号产品在有效期内的质量稳定性,还是不同批号产品质量的持续稳定性均符合预期。
3 结论
本文对选取或设定的湿式大肠菌群快检纸片的污染指标、特异性指标、检出水平(LODX)、检测结果有效性和产品质量稳定性等5项性能指标进行了较为详细的试验分析,证明该纸片性能稳定可靠,符合要求和预期的同时,也表明本文所探索的对湿式大肠菌群快检纸片性能进行分析验证的一般流程可有效的对该类纸片产品进行较为全面的性能验证,在使用该类快检产品时可作为产品选用和验收、验证的参考。
参考文献
[1]何国庆,贾英民,丁立孝.食品微生物学[M].北京:中国农业大学出版社,2016.
[2]刘德鹏,郝英敏,姜玉芳.湿式与干式大肠菌群快检纸片的应用比较研究[J].医药前沿,2015(28):172-174.
[3]王珍,陆雯,吴岳琴,等.四种大肠菌群快速检测纸片质量考察[J].现代食品,2019,12(23):138-142.
[4]王赞信.大肠菌群快检纸片的质量检测分析[J].预防医学,2005,17(5):81-82.
[5]国家认证认可监督管理委员会.微生物检测方法确认与验证指南:RB/T 033—2020[S].北京:中国标准出版社,2016.
热点推荐
-

主要食品配料厂商携手支持可持续农业
-

别样肉客在华推出脆香酥炸植物基蟹饼,为新春佳节增添美食新选
-

ADM首度亮相FBIF2023,探索食品饮料的今天、明天和未来
-

专访婴儿水团体标准制定者:为何为婴儿饮用水制定更高标准?
-

使用梅特勒-托利多X光机的五大理由
-

广西发动全区3·15食品安全“你点我检 服务惠民生”问卷调查
-

河南全省食品安全监管工作会议在鹤壁召开
-

万里挑一的“进博TOP好物”,三养创新产品与食安承诺受赞誉
-

河南省餐饮食品安全“总监话总监”巡讲活动在洛阳启动
-

郑州市举办2024年“质量月”质量诚信进商超暨质量提升交流观摩会
-

仁和中方医药股份联合民生大药房送健康捐赠活动在郑州举行
-

三养密阳工厂深度揭秘:火鸡面的食品安全与品质卓越之道
-

郑州市金水区召开学校食堂承包经营企业 食品安全行政指导会
-

陕西省举办全省学校食堂食品安全管理及投诉处置现场会
-

山西省局举办质量提升行动助力汾酒专业镇高质量发展活动
-

郑州市金水区开展肉类产品质量安全专项整治
-

郑州市市场监管局开展网络餐饮服务食品安全行政指导工作
-

西藏山南市率先将“两个责任”进党校 推动食品安全社会共治
-

湖北:开展校园食品安全和“五一” 期间食品安全监管工作
-

河南省政府食品安全办召开2024年夏季食品安全形势会商会议
-

山西省局召开食品安全抽检承检机构任务部署会
-

南昌市开展春节前食品经营安全监督检查
-

河南省汝南县:“你点我检服务惠民生”护航“双节”食品安全
-

湖北省局推动共建“外卖小哥食堂” 让外卖骑手暖心又暖胃
-

焦作市校园食品安全排查整治专项行动动员部署会召开
-

汝南县市场监管局“四个抓手”提升集中用餐单位食品安全水平
-

山西省市场监管局食品案件查办指导中心正式挂牌运行
-

河南省汝南县市场监管局多措并举开展学校食堂食品安全评价
-

恩施州市场监管局服务第八届世界硒博会
-

开封市市场监管局2023年食品抽检工作质量提升推进会召开





