影响白酒中氰化物检测加标回收率因素 探究及方法优化
2019-08-28 13:30:13 来源: 食品安全导刊
摘要:按照国标GB 5009.36-2016中第一法对白酒中进行氰化物检测发现样品加标回收率偏低,且检测结果不太稳定。通过实验研究,发现由于加入碱液浓度过低、加热时长过长造成碱性条件下加热除去高沸点有机物过程中出现目标物氰化物损失,同时发现样品中含有酒精度、总酸、总酯含量、加标浓度变化均可造成回收率变化,最终通过提高碱液浓度到10g/L,缩短加热时长至30min,添加硼氢化钾等方式确保回收率达到85%以上且检测结果稳定。
关键词:白酒;氰化物;加标回收率;碱液浓度;加热时长
氰化物是酒类的一项重要食品安全指标。白酒中氰化物来源有很多种:如果白酒在酿造过程中使用了使用木薯和薯类植物为原料,根部外表大量氢氰酸会导致氰化物产生,酿酒过程中可能使用了受污染生产用水、使用含氰化物基酒或调味酒[1]、使用农药污染的原料和酿酒过程中的变异反应[2]都有可能带入氰化物污染,所以白酒氰化物超标时有发生。GB2757-2017中规定氰化物(以HCN计按100%酒精度折算)限量≤8.0mg/kg[3]。GB 5009.36-2016中第一法紫外分光光度法是白酒中氰化物检测最常用的检测方法,与被替代方法GB 5009.48-2003的4.7相比,新方法采用碱性条件下加热除去高沸点有机物,然后在pH=7.0条件下,用氯胺T将氰化物转变为氯化氰,再与异烟酸-吡唑啉酮作用,生成蓝色染料,与标准系列比较定量的原理,主要优化了检测过程中部分样品在显色过程中由于高沸点有机物引起的显色液浑浊问题,即GB 5009.36-2016中第一法的5.2.1步骤:“吸取1.0mL试样于50mL烧杯中,加入5mL2g/L氢氧化钠溶液,放置10min,然后放于120℃电加热板上加热至溶液剩余约1mL,取下放至室温,用2g/L氢氧化钠溶液转移至10mL具塞比色管中,最后加2g/L氢氧化钠至5mL”[4][5]。但在实际检测过程中发现由于该步骤中对于“120℃电加热板上加热至溶液剩余约1mL”最终剩余溶液体积没有强调精确,所以在实际检测过程中就会出现相同样品在加热后最终剩余溶液体积(相同加热条件下通过加热时长反映)不同引起检测结果不一致的情况。同时在检测中还发现严格按照该步骤操作,将溶液120℃电加热板上加热至溶液<2ml时,大部分白酒样品加标回收率都很低且不同白酒样回收率差异较大。为探究检测过程中对白酒中氰化物含量检测影响因素,针对GB 5009.36-2016中第一法的5.2.1步骤进行相关探索实验。
1.实验方法与材料:
1.1实验材料:
1.1.1试剂:蒸馏水,无水乙醇,冰醋酸,乙酸乙酯、氢氧化钠系列溶液(18g/L,15g/L,12g/L,10g/L,5g/L,2g/L),硼氢化钾碱溶液(0.3g硼氢化钾溶于100ml 2g/L氢氧化钠溶液中),2g/L乙酸溶液(1+24),酚酞-乙醇指示液(10g/L),磷酸盐缓冲溶液[(0.5mol/L)pH7.0],异烟酸-吡唑啉酮溶液, 氯胺T溶液(10g/L),水中氰成分分析标准物质(50μg/mL),氰离子标准中间液(1μg/mL)。
1.1.2仪器、器皿:双光束紫外可见分光光度计(TU1900北京普析通用仪器有限责任公司),电热恒温水浴锅(北京市光明医疗仪器有限公司),电加热板(DB-3金坛市金城国盛实验仪器厂),千分之一电子天平(JY203上海浦春计量仪器有限公司),50ml玻璃烧杯, 10mL具塞比色管,25mL具塞比色管。
1.1.3 样品:
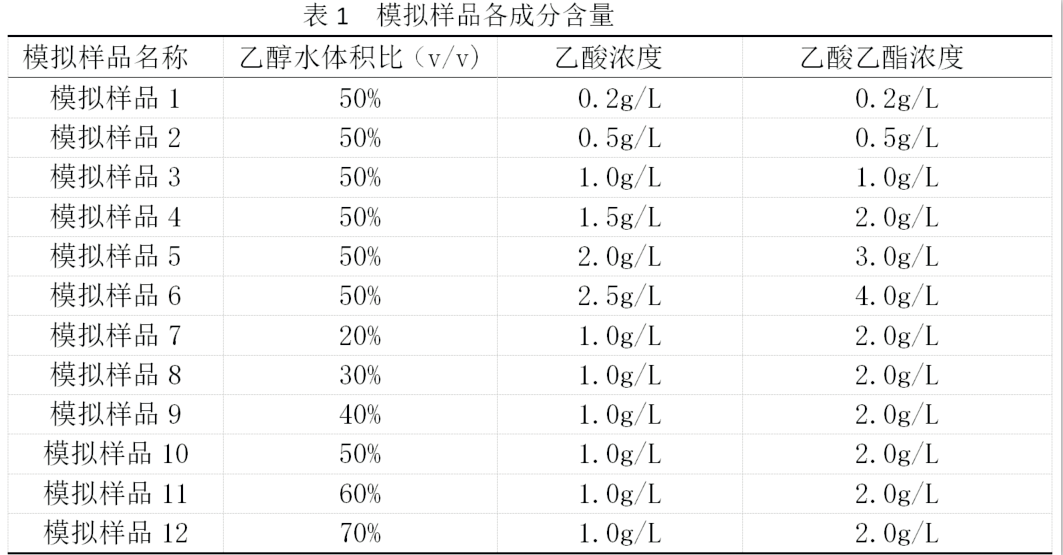
1.1.1.1市售不同类型白酒
1.1.1.2模拟白酒样品:使用无水乙醇、蒸馏水、乙酸、乙酸乙酯配制的模拟白酒样品
1.2实验方法:
1.2.1检测加热时长对加标回收率的影响(反映最终加热后剩余液体)
在相同的条件下,即加热温度、加热板、被测样品,全部一致的情况下,通过不同的加热时长处理(20min,30min,40min,50min,60min,70min,80min)。实验操作除了5.2.1步骤“于120℃电加热板上加热至溶液剩余约1mL,”外,其余步骤按照GB 5009.36-2016中第一法操作。通过样品加标回收实验,检测不同三种白酒样品在不同加热时长下样品回收率。
1.2.2检测加入碱液浓度及标品添加浓度对加标回收率的影响
在相同的条件下,通过加入5ml不同浓度浓度氢氧化钠溶液(2g/L,5g/L,10g/L,15g/L,18g/L),即加热温度、加热时长、加热板、被测样品全部一致的情况下,实验操作除了5.2.1步骤“加入5mL2g/L 氢氧化钠溶液”外,其余步骤按照GB 5009.36-2016中第一法操作。通过样品加标回收实验,检测不同三种白酒样品在相同加热时长下样品回收率。
在相同情况下,按照GB 5009.36-2016中第一法操作步骤,对三个白酒样品添加不同量的标品,检测样品在标品不同添加浓度下的加标回收率,检测标品添加浓度对加标回收率的影响。
1.2.3样品中总酸总酯及酒精度对加标回收率影响
在相同情况下,按照GB 5009.36-2016中第一法操作步骤,对模拟样品1-12号进行样品加标检测,检测相同酒精度样品中总酸总酯对加标回收率影响及相同总酸总酯条件下乙醇与水的体积比(体现酒精度)对加标回收率影响。
1.2.4 对方法优化后加标回收率的检测
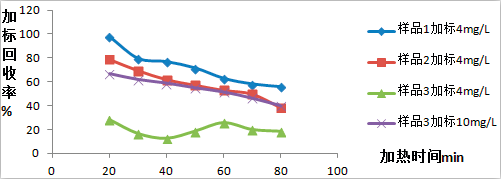
图表 1不同加热时长对加标回收率影响
通过提高氢氧化钠浓度、缩短加热时长、添加还原剂的方式对检测方法进行优化,检测不同样品的加标回收率,找到最合适的检测方法。
2.检测数据与结果分析:
2.1检测加热时长对加标回收率的影响(反映加热后剩余溶液体积)
通过图表1实验数据发现:除了白酒样品3在加标浓度4mg/L时,由于整体回收率太低,导致检测结果低看不出明显趋势;样品1和样品2回收率随着加热时长增加,其加标回收率呈下降趋势。样品3在将加标浓度增加到10mg/L后,随加热时长增加,其加标回收率也呈下降趋势。即白酒样品的加标回收率随加热剩余液体体积的减少而减少,当加热时长达到80min时,剩余液体<2ml才能保证达到GB 5009.36-2016中第一法的5.2.1步骤中“加热至溶液剩余约1mL”,而此时大部分样品加标回收率低于60%,部分样品低于40%,通过缩短加热时长确实可以提高样品加标回收率,但是像样品3这样的白酒样品,加热时间低于30min会因为部分高沸点有机物(主要是醛类)挥发不彻底,导致后续步骤显色过程出现浑浊,出现显色偏浅,所以仅仅缩短加热时长无法获得满意的加标回收率,这种变化趋势在氰化物阳性样品中也存在,实验数据见图表2。

图表 2 阳性样品的氰化物含量随加热时长变化
2.2检测加入碱液浓度及标品添加浓度对加标回收率的影响
通过图表3实验数据可知,确实可以通过提高加入固定氰化物的碱液浓度减少加热过程中氰化物损失来提高添加回收率,但是加入碱液到达一定浓度后可能影响到后续显色,且对于下一步调节pH值带来困难,所以大部分样品在大约10g/L的氢氧化钠浓度下具有最高添加回收率,再增加氢氧化钠浓度后添加回收率反而会下降,且仅提高氢氧化钠浓度不足以达到满意的加标回收率。

图表 3 不同碱液浓度对加标回收率的影响
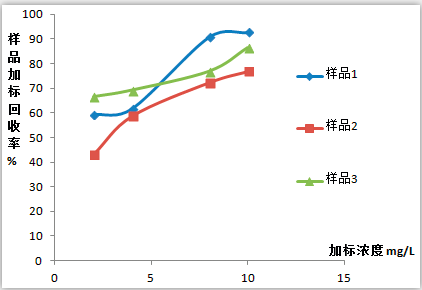
图表 4不同加标浓度对加标回收率的影响
而根据图表4实验数据可知在检测真实酒样过程中,标品添加浓度越高的情况下,回收率越高。这就解释了在检测过程中相同的酒样在不同的标品添加浓度下为何会造成添加回收率存在很大的差异,主要原因可能是不同浓度下氰化物损失速率不同造成的。
2.3检测样品中酒精度及总酸总酯对加标回收率影响
通过图表6实验数据可知,对模拟样品的加标回收率检测,在相同的酒精度(乙醇水体积比体现)情况下,总酸、总酯含量越高,样品加标回收率越低。可能原因是样品中的总酸、总酯会消耗溶液中的氢氧化钠,影响碱液中对氰化物的固定 。

图表6 50%(V/V)乙醇模拟样品在不同总酸、总酯浓度下加标回收率影响
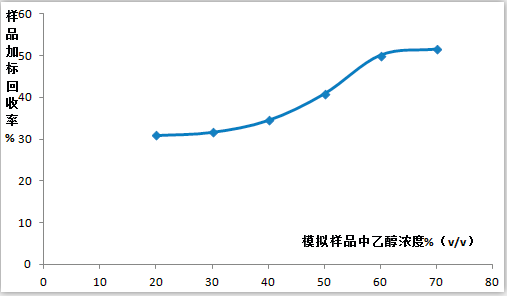
图表7 不同体积比乙醇模拟样品在相同总酸、总酯浓度下加标回收率影响
通过图表7实验数据可知,对模拟样品的加标回收率检测,在总酸、总酯含量相同的情况下,乙醇水体积比(体现酒精度)越高,加标回收率越高。
2.4 对方法优化后加标回收率检测
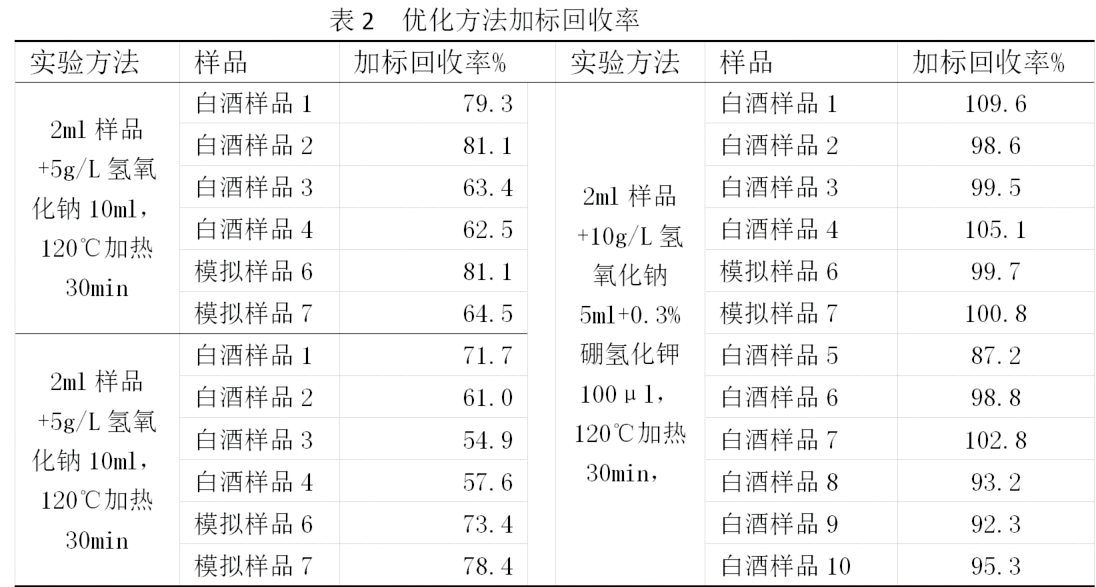
通过上述实验确定影响白酒中氰化物检测影响因素很多,试验中我们可控的因素只有两种:即加热时长(剩余溶液体积)和调节氢氧化钠浓度,根据验证数据,减少加热时长和将氢氧化钠调节到合适浓度,可以提高加标回收率,且单独优化一个因子无法保证所有样品具有较高回收率。另外在实际操作中,按照GB 5009.36-2016中第一法的5.2.1步骤操作,在减少加热时长同时,由于剩余溶液体积增加,导致后续步骤中最终定容体积会超过规定的10ml,所以优化方法将步骤中各液体体积扩大一倍,定容体积增至25ml可解决这一问题(后通过实验发现碱液体积为5ml对检测结果也未有明显影响)。另外,由于部分含醛类物质较多的白酒,加热时长太短会造成后续显色过程浑浊,导致显色偏浅,结果偏低,加热时长太长又会造成氰化物损失,通过实验确认加入一定量的硼氢化钾还原白酒中醛类物质可以解决在加热时间较短时显色浑浊问题。最终确定如下操作步骤可以保证大多数被测样品加标回收率能在95%以上,所有被测样品加标回收率在85%以上,具体操作步骤如下:
(1)吸取2.0mL试样于50mL 烧杯中,加入5mL 10g/L 氢氧化钠溶液和0.3%硼氢化钾100μl,放置10min,然后放于120℃电加热板上加热30min,取下放至室温,用水转移至25mL具塞比色管中,加水至10mL;
(2)用移液管分别吸取0mL、0.5mL、1mL、2mL、4mL、6mL氰离子标准中间液置于25mL比色管中,加水至10mL。
(3)于试样及标准管中分别加入2滴酚酞指示剂,然后加入乙酸溶液调至红色褪去,再用2g/L氢氧化钠溶液调至近红色,然后加4mL磷酸盐缓冲溶液(如果室温低于20 ℃即放入25 ℃~30 ℃水浴中10min),再加入0.4mL氯胺T溶液,摇匀放置3min,加入4mL异烟酸-吡唑啉酮溶液,加水稀释至刻度,加塞混合均匀,在37℃恒温水浴锅中放置40min,取出用1cm 比色杯以空白管调节零点,于波长638nm 处测吸光度。
3.结论:
根据实验,我们得出如下结论:按照GB 5009.36-2016 第一法检测白酒氰化物过程中,之所以会出现样品检测结果不稳定的原因是:该方法并未精确规定加热剩余液体的体积,而加热后剩余溶液体积的多少会对检测结果有影响;之所以会出现加标回收率偏低且不稳定的问题,主要是因为加热后剩余溶液多少,样品中标品添加浓度,酒样中酒精度、总酸、总酯含量不一致都会对样品加标回收率造成影响。究其原因主要是因为加入氢氧化钠浓度过低,加热时长过长导致加热过程中出现氰化物损失。通过实验可知,即使增加碱液浓度,也无法在加热至溶液只剩约1ml的情况下保证有很好的加标回收率,说明碱液固定氰化物在长时间加热时并不稳定。而仅仅通过提高加入的碱液浓度或缩短加热时长,也无法保证检测结果稳定,但如果通过同时提高加入的氢氧化钠浓度和缩短加热时长并加入强还原剂硼氢化钾情况下,可以使绝大多数白酒样品具有较高加标回收率且检测结果稳定。
参考文献:
[1]徐新江 白酒中氰化物来源分析与处理方法 酿酒科技 2017NO.10(TOL.280):90-91
[2]沈祖志 李华侨 范信亮 酒中氰化物处理机制研制成功 酿酒科技 2014.12.18
[3] 中华人民共和国卫生部。GB 2757-2012 食品安全国家标准 蒸馏酒及其配制酒[s]
[4]中华人民共和国卫生部,中国国家标准化管理委员会。GB/T 5009.48-2003 蒸馏酒与配制酒卫生标准分析方法[s]
[5] 中华人民共和国国家卫生和计划生育委员会,国家食品药品监督管理总局。GB 5009.36-2016 食品安全国家标准 食品中氰化物的测定[s]
杨军 常德市食品检验所
热点推荐
-

主要食品配料厂商携手支持可持续农业
-

别样肉客在华推出脆香酥炸植物基蟹饼,为新春佳节增添美食新选
-

ADM首度亮相FBIF2023,探索食品饮料的今天、明天和未来
-

专访婴儿水团体标准制定者:为何为婴儿饮用水制定更高标准?
-

使用梅特勒-托利多X光机的五大理由
-

广西发动全区3·15食品安全“你点我检 服务惠民生”问卷调查
-

河南全省食品安全监管工作会议在鹤壁召开
-

万里挑一的“进博TOP好物”,三养创新产品与食安承诺受赞誉
-

河南省餐饮食品安全“总监话总监”巡讲活动在洛阳启动
-

郑州市举办2024年“质量月”质量诚信进商超暨质量提升交流观摩会
-

仁和中方医药股份联合民生大药房送健康捐赠活动在郑州举行
-

三养密阳工厂深度揭秘:火鸡面的食品安全与品质卓越之道
-

郑州市金水区召开学校食堂承包经营企业 食品安全行政指导会
-

陕西省举办全省学校食堂食品安全管理及投诉处置现场会
-

山西省局举办质量提升行动助力汾酒专业镇高质量发展活动
-

郑州市金水区开展肉类产品质量安全专项整治
-

郑州市市场监管局开展网络餐饮服务食品安全行政指导工作
-

西藏山南市率先将“两个责任”进党校 推动食品安全社会共治
-

湖北:开展校园食品安全和“五一” 期间食品安全监管工作
-

河南省政府食品安全办召开2024年夏季食品安全形势会商会议
-

山西省局召开食品安全抽检承检机构任务部署会
-

南昌市开展春节前食品经营安全监督检查
-

河南省汝南县:“你点我检服务惠民生”护航“双节”食品安全
-

湖北省局推动共建“外卖小哥食堂” 让外卖骑手暖心又暖胃
-

焦作市校园食品安全排查整治专项行动动员部署会召开
-

汝南县市场监管局“四个抓手”提升集中用餐单位食品安全水平
-

山西省市场监管局食品案件查办指导中心正式挂牌运行
-

河南省汝南县市场监管局多措并举开展学校食堂食品安全评价
-

恩施州市场监管局服务第八届世界硒博会
-

开封市市场监管局2023年食品抽检工作质量提升推进会召开





